第七章素养检测
一、刷速度
1.人类的衣、食、住、行离不开有机物。下列说法错误的是( )
A. 向鸡蛋清溶液中加入几滴浓硝酸并加热,蛋白质会发生显色反应,用于蛋白质的检验
B. 煤的干馏、气化、液化均为化学变化
C. 糖类、油脂、蛋白质都是天然有机高分子,在一定条件下都能发生水解
D. 阿司匹林(乙酰水杨酸)是一种合成药物,水解产物中的水杨酸会刺激胃黏膜,长期大量服用对人体有害
答案:C
解析:向鸡蛋清溶液中加入浓硝酸并加热会发生显色反应(黄色),这是蛋白质的颜色反应,可用于检验蛋白质, $ {\rm \mathrm{A}} $ 正确;煤的干馏(分解生成新物质)、气化(转化为 $ {\rm \mathrm{C}\mathrm{O}} $ 和 $ {\rm {\mathrm{H}}_{2}} $ )、液化(转化为液体燃料)均涉及化学变化, $ {\rm \mathrm{B}} $ 正确;糖类中的单糖(如葡萄糖)和油脂均为小分子化合物,且单糖不能水解, $ {\rm \mathrm{C}} $ 错误;阿司匹林水解生成水杨酸,其对胃黏膜有刺激性,长期大量服用对人体有害, $ {\rm \mathrm{D}} $ 正确。
2.下列关于有机物的说法正确的是( )
①可以用蒸馏的方法分离 $ {\rm {\mathrm{B}\mathrm{r}}_{2}} $ 和 $ {\rm {\mathrm{C}\mathrm{C}\mathrm{l}}_{4}} $
②可以用酸性高锰酸钾溶液除去 $ {\rm {\mathrm{C}\mathrm{O}}_{2}} $ 气体中的乙烯
③乙烯、聚氯乙烯均能使溴的 $ {\rm {\mathrm{C}\mathrm{C}\mathrm{l}}_{4}} $ 溶液褪色
④乙醇、乙酸、乙酸乙酯都能发生取代反应
⑤鸡蛋清溶液遇醋酸铅溶液发生盐析
A. ①②④
B. ①④⑤
C. ③④⑤
D. ②③⑤
答案:A
解析: $ {\rm {\mathrm{B}\mathrm{r}}_{2}} $ 和 $ {\rm {\mathrm{C}\mathrm{C}\mathrm{l}}_{4}} $ 的沸点不同,可以用蒸馏的方法分离,①正确;乙烯可被酸性高锰酸钾溶液氧化成二氧化碳,不会引入新杂质,②正确;聚氯乙烯不含碳碳双键,不能使溴的 $ {\rm {\mathrm{C}\mathrm{C}\mathrm{l}}_{4}} $ 溶液褪色,③错误;乙醇、乙酸、乙酸乙酯都能发生取代反应,④正确;醋酸铅为重金属盐,鸡蛋清溶液遇醋酸铅溶液变性,⑤错误;选 $ {\rm \mathrm{A}} $ 。
3.两种气态烃组成的混合气体完全燃烧后所得到 $ {\rm {\mathrm{C}\mathrm{O}}_{2}} $ 和 $ {\rm {\mathrm{H}}_{2}\mathrm{O}} $ 的物质的量随混合烃总物质的量的变化如图所示,下列有关混合气体的说法正确的是( )
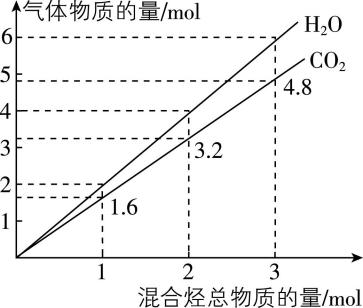
A. 该混合气体中一定含有乙烷
B. 该混合气体一定含有甲烷和乙炔
C. 若混合气体由 $ {\rm {\mathrm{C}\mathrm{H}}_{4}} $ 和 $ {\rm {\mathrm{C}}_{2}{\mathrm{H}}_{4}} $ 组成,则其体积比为 $ 1:3 $
D. 在 $ 110℃ $ 条件下,混合气体与氧气混合,总混合气燃烧前后压强不变
答案:D
解析:由分析知,该混合气体中一定不含乙烷、乙炔, $ {\rm \mathrm{A}} $ 、 $ {\rm \mathrm{B}} $ 错误;相同条件下气体的体积之比等于气体的物质的量之比,若混合气体由 $ {\rm {\mathrm{C}\mathrm{H}}_{4}} $ 和 $ {\rm {\mathrm{C}}_{2}{\mathrm{H}}_{4}} $ 组成,令甲烷物质的量为 $ a\mathrm{m}\mathrm{o}\mathrm{l} $ 、乙烯为 $ b\mathrm{m}\mathrm{o}\mathrm{l} $ ,两种气态烃的平均组成为 $ {\rm {\mathrm{C}}_{1.6}{\mathrm{H}}_{4}} $ 时, $ \dfrac{a+2b}{a+b}=1.6 $ ,整理得 $ a:b=2:3 $ , $ {\rm \mathrm{C}} $ 错误;在 $ 110℃ $ 条件下,生成的水为气体,由烃的燃烧通式知, $ 1+(1.6+\dfrac{4}{4})=1.6+\dfrac{4}{2} $ ,则燃烧前后压强不变, $ {\rm \mathrm{D}} $ 正确。
4. 4.苹果酸结构简式为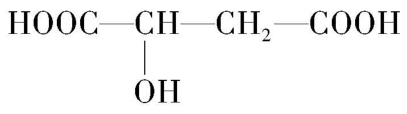 。下列相关说法不正确的是( )
。下列相关说法不正确的是( )
A. $ 1\mathrm{m}\mathrm{o}\mathrm{l} $ 苹果酸与足量 $ {\rm \mathrm{N}\mathrm{a}} $ 反应生成标准状况下 $ {\rm 11.2\mathrm{L}{\mathrm{H}}_{2}} $
B. 苹果酸在一定条件下能发生催化氧化反应
C. $ 1\mathrm{m}\mathrm{o}\mathrm{l} $ 苹果酸与 $ {\rm {\mathrm{N}\mathrm{a}\mathrm{H}\mathrm{C}\mathrm{O}}_{3}} $ 溶液反应,最多消耗 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{N}\mathrm{a}\mathrm{H}\mathrm{C}\mathrm{O}}_{3}} $
D. 苹果酸能发生酯化反应的官能团有羧基和羟基
答案:A
解析:羧基和羟基均能与 $ {\rm \mathrm{N}\mathrm{a}} $ 反应, $ 1\mathrm{m}\mathrm{o}\mathrm{l} $ 苹果酸与足量 $ {\rm \mathrm{N}\mathrm{a}} $ 反应生成 $ {\rm 1.5\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{H}}_{2}} $ ,标准状况下体积为 $ {\rm 33.6\mathrm{L}} $ , $ {\rm \mathrm{A}} $ 错误;苹果酸中羟基所连碳原子上有 $ {\rm \mathrm{H}} $ ,在一定条件下能发生催化氧化反应生成酮, $ {\rm \mathrm{B}} $ 正确; $ 1\mathrm{m}\mathrm{o}\mathrm{l} $ 苹果酸含有 $ 2\mathrm{m}\mathrm{o}\mathrm{l} $ 羧基,与 $ {\rm {\mathrm{N}\mathrm{a}\mathrm{H}\mathrm{C}\mathrm{O}}_{3}} $ 溶液反应,最多消耗 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{N}\mathrm{a}\mathrm{H}\mathrm{C}\mathrm{O}}_{3}} $ , $ {\rm \mathrm{C}} $ 正确;苹果酸中 $ {\rm —\mathrm{O}\mathrm{H}} $ 与 $ {\rm —\mathrm{C}\mathrm{O}\mathrm{O}\mathrm{H}} $ 均能发生酯化反应, $ {\rm \mathrm{D}} $ 正确。
5.下列由实验得出的结论正确的是( )
选项 | 实验 | 结论 |
A | 甲烷与氯气在光照下反应后的混合气体能使湿润的蓝色石蕊试纸变红 | 生成的一氯甲烷具有酸性 |
B | 向淀粉溶液中加入少量稀硫酸,加热 $ 4\sim 5 \min $ ,冷却后向其中加入新制 $ {\rm \mathrm{C}\mathrm{u}(\mathrm{O}\mathrm{H})_{2}} $ ,加热,无砖红色沉淀 | 淀粉没有发生水解 |
C | 将石蜡分解产生的气体通入酸性高锰酸钾溶液,溶液褪色 | 石蜡分解产生乙烯 |
D | 将乙烯通入溴的四氯化碳溶液,溶液最终变为无色透明 | 发生加成反应,产物无色、可溶于四氯化碳 |
解析:甲烷和氯气发生取代反应生成的 $ {\rm \mathrm{H}\mathrm{C}\mathrm{l}} $ 具有酸性,能使湿润的蓝色石蕊试纸变红, $ {\rm \mathrm{A}} $ 错误;检验淀粉是否发生水解,向淀粉溶液中加少量稀硫酸,加热 $ 4\sim 5 \min $ ,冷却后应先加氢氧化钠溶液中和硫酸,将溶液调至碱性,再加入新制 $ {\rm \mathrm{C}\mathrm{u}(\mathrm{O}\mathrm{H})_{2}} $ 加热, $ {\rm \mathrm{B}} $ 错误;将石蜡分解产生的气体通入酸性高锰酸钾溶液,溶液褪色,说明石蜡分解产生了不饱和烃,但不一定是乙烯, $ {\rm \mathrm{C}} $ 错误;将乙烯通入溴的四氯化碳溶液,乙烯和溴发生加成反应生成 $ {\rm 1,} 2- $ 二溴乙烷,溶液最终变为无色透明,说明 $ {\rm 1,} 2- $ 二溴乙烷无色且可溶于四氯化碳, $ {\rm \mathrm{D}} $ 正确。
6.纤维素的单链结构如图。下列说法正确的是( )
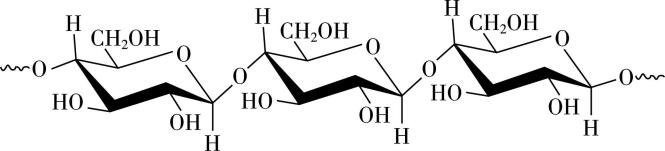
A. 纤维素能发生氧化反应和酯化反应
B. 纤维素水解可以直接得到乙醇
C. 纤维素在常温稀碱溶液中可以大量水解
D. 纤维素遇碘单质变蓝
答案:A
解析:纤维素结构中含有羟基,且羟基所连碳原子上有氢原子,能发生氧化反应,也可发生酯化反应, $ {\rm \mathrm{A}} $ 正确;纤维素水解产物是葡萄糖,不能直接得到乙醇, $ {\rm \mathrm{B}} $ 错误;纤维素在常温、稀碱溶液中水解程度很小, $ {\rm \mathrm{C}} $ 错误;纤维素遇碘单质不变蓝, $ {\rm \mathrm{D}} $ 错误。
7. 7.已知: $ {\rm \mathrm{R}-\mathrm{C}\equiv \mathrm{C}-\mathrm{H}+\mathrm{R}\prime \mathrm{B}\mathrm{r}{\xrightarrow[ ~]{一定条件}}\mathrm{R}-\mathrm{C}\equiv \mathrm{C}-\mathrm{R}\prime +\mathrm{H}\mathrm{B}\mathrm{r}(\mathrm{R}} $ 表示氢原子或烃基, $ {\rm \mathrm{R}\prime} $ 表示烃基 $ ) $ ,利用该反应合成的导电高分子材料 $ {\rm \mathrm{P}} $ 的结构为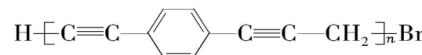 。下列说法不正确的是( )
。下列说法不正确的是( )
A. 炔烃和卤代烃在一定条件下可发生取代反应
B. 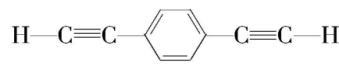 和苯乙炔不互为同系物
和苯乙炔不互为同系物
C. 高分子材料 $ {\rm \mathrm{P}} $ 能使溴的四氯化碳溶液褪色
D. 生成 $ {\rm \mathrm{P}} $ 的单体是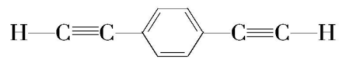 和 $ {\rm {\mathrm{C}\mathrm{H}}_{3}\mathrm{B}\mathrm{r}} $
和 $ {\rm {\mathrm{C}\mathrm{H}}_{3}\mathrm{B}\mathrm{r}} $
答案:D
解析: $ {\rm \mathrm{R}-\mathrm{C}\equiv \mathrm{C}-\mathrm{H}+\mathrm{R}\prime \mathrm{B}\mathrm{r}{\xrightarrow[ ~]{一定条件}}\mathrm{R}-\mathrm{C}\equiv \mathrm{C}-\mathrm{R}\prime +\mathrm{H}\mathrm{B}\mathrm{r}} $ ,此反应的反应类型为取代反应, $ {\rm \mathrm{A}} $ 正确;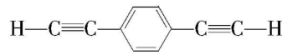 分子中含有两个碳碳三键,苯乙炔分子中只含有一个碳碳三键,二者结构不相似,不互为同系物, $ {\rm \mathrm{B}} $ 正确;高分子材料 $ {\rm \mathrm{P}} $ 中含有碳碳三键,能使溴的四氯化碳溶液褪色, $ {\rm \mathrm{C}} $ 正确;生成 $ {\rm \mathrm{P}} $ 的单体是
分子中含有两个碳碳三键,苯乙炔分子中只含有一个碳碳三键,二者结构不相似,不互为同系物, $ {\rm \mathrm{B}} $ 正确;高分子材料 $ {\rm \mathrm{P}} $ 中含有碳碳三键,能使溴的四氯化碳溶液褪色, $ {\rm \mathrm{C}} $ 正确;生成 $ {\rm \mathrm{P}} $ 的单体是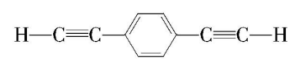 和 $ {\rm {\mathrm{C}\mathrm{H}}_{2}{\mathrm{B}\mathrm{r}}_{2}} $ , $ {\rm \mathrm{D}} $ 错误。
和 $ {\rm {\mathrm{C}\mathrm{H}}_{2}{\mathrm{B}\mathrm{r}}_{2}} $ , $ {\rm \mathrm{D}} $ 错误。
8. 8.利用有机分子模拟生物体内“醛缩酶”催化共轭双烯与烯烃或炔烃发生加成反应生成六元环状化合物的反应(称为 $ {\rm \mathrm{D}\mathrm{i}\mathrm{e}\mathrm{l}\mathrm{s}-\mathrm{A}\mathrm{l}\mathrm{d}\mathrm{e}\mathrm{r}} $ 反应,如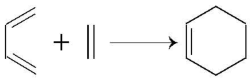 )取得重要进展。某 $ {\rm \mathrm{D}\mathrm{i}\mathrm{e}\mathrm{l}\mathrm{s}-\mathrm{A}\mathrm{l}\mathrm{d}\mathrm{e}\mathrm{r}} $ 反应由Ⅰ和Ⅲ反应生成Ⅴ的催化机理如图所示( $ {\rm —{\mathrm{C}\mathrm{O}}_{2}\mathrm{M}\mathrm{e}} $ 即 $ {\rm —{\mathrm{C}\mathrm{O}\mathrm{O}\mathrm{C}\mathrm{H}}_{3}} $ 、 $ {\rm —\mathrm{B}\mathrm{n}} $ 即
)取得重要进展。某 $ {\rm \mathrm{D}\mathrm{i}\mathrm{e}\mathrm{l}\mathrm{s}-\mathrm{A}\mathrm{l}\mathrm{d}\mathrm{e}\mathrm{r}} $ 反应由Ⅰ和Ⅲ反应生成Ⅴ的催化机理如图所示( $ {\rm —{\mathrm{C}\mathrm{O}}_{2}\mathrm{M}\mathrm{e}} $ 即 $ {\rm —{\mathrm{C}\mathrm{O}\mathrm{O}\mathrm{C}\mathrm{H}}_{3}} $ 、 $ {\rm —\mathrm{B}\mathrm{n}} $ 即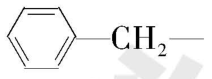 )。下列说法正确的是( )
)。下列说法正确的是( )
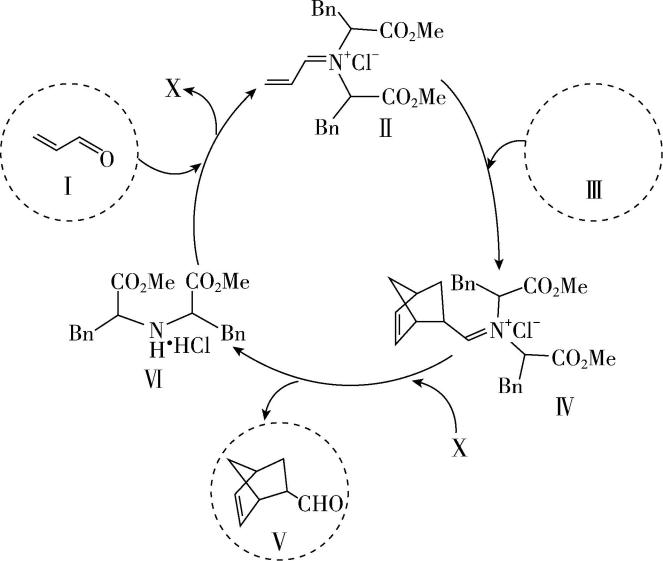
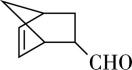
A. Ⅲ的结构简式为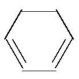
B. Ⅰ和Ⅴ互为同系物
C. 化合物 $ Ⅹ $ 为 $ {\rm {\mathrm{H}}_{2}\mathrm{O}} $
D. Ⅳ是反应的催化剂
答案:C
9.学生在实验室制取乙酸乙酯的装置如图。下列说法错误的是( )
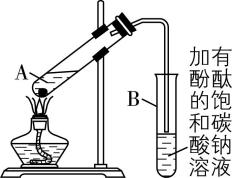
A. 若用含示踪原子 $ {\rm {}^{18}\mathrm{O}} $ 的乙醇和乙酸反应,则A中反应方程式: $ {\rm {\mathrm{C}\mathrm{H}}_{3}\mathrm{C}\mathrm{O}\mathrm{O}\mathrm{H}+{\mathrm{C}}_{2}{\mathrm{H}}_{5}^{18}\mathrm{O}\mathrm{H}\stackrel{浓硫酸}{\underset{△}{⇌}}{\mathrm{C}\mathrm{H}}_{3}{\mathrm{C}\mathrm{O}}^{18}{\mathrm{O}\mathrm{C}}_{2}{\mathrm{H}}_{5}+{\mathrm{H}}_{2}\mathrm{O}} $
B. 长导管不伸入饱和碳酸钠液面以下的目的是防倒吸
C. 分离出乙酸乙酯层用的方法是分液
D. 如果用 $ 4.6\mathrm{g} $ 的 $ {\rm {\mathrm{C}}_{2}{\mathrm{H}}_{5}\mathrm{O}\mathrm{H}} $ 和 $ 9.0\mathrm{g} $ 的乙酸反应制得乙酸乙酯 $ 6.6\mathrm{g} $ ,则本实验的产率是 $ 50\% $
答案:D
解析:酯化反应的机理是酸脱羟基醇脱氢, $ {\rm \mathrm{A}} $ 正确;导管伸入液面以下可能会发生倒吸, $ {\rm \mathrm{B}} $ 正确;乙酸乙酯是有机物,难溶于水且密度比水小,静置后分层且乙酸乙酯在上层,分液可分离出来, $ {\rm \mathrm{C}} $ 正确; $ 4.6\mathrm{g}(0.1\mathrm{m}\mathrm{o}\mathrm{l}) $ 的 $ {\rm {\mathrm{C}}_{2}{\mathrm{H}}_{5}\mathrm{O}\mathrm{H}} $ 和 $ 9.0\mathrm{g}(0.15\mathrm{m}\mathrm{o}\mathrm{l}) $ 的乙酸反应,乙酸过量,因此使用乙醇的量进行计算,乙醇的物质的量为 $ 0.1\mathrm{m}\mathrm{o}\mathrm{l} $ ,理论上完全反应生成乙酸乙酯的物质的量为 $ 0.1\mathrm{m}\mathrm{o}\mathrm{l} $ ,即 $ 8.8\mathrm{g} $ ,因此产率为 $ \dfrac{6.6\mathrm{g}}{8.8\mathrm{g}}×100\%=75\% $ , $ {\rm \mathrm{D}} $ 错误。
10.地沟油的主要成分是油脂,它可以通过多种方式转化为有用的资源。以地沟油为原料制备有机高分子材料 $ {\rm \mathrm{E}(\mathrm{P}\mathrm{V}\mathrm{A})} $ 和具有水果香味的有机物 $ {\rm \mathrm{F}} $ 过程中的转化关系如下:
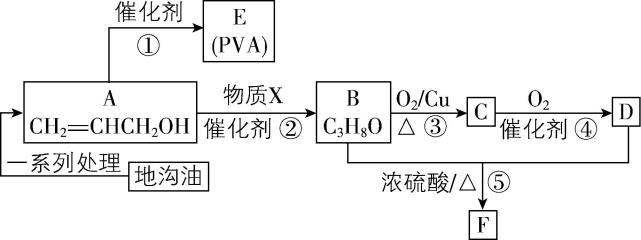
(1) 反应②的原子利用率为 $ 100\% $ ,物质 $ {\rm \mathrm{X}} $ 的化学式为 ,D中的官能团名称为 。
(2) 根据有机物A的结构特征,分析预测其可能的化学性质,完成下表。
序号 | 反应试剂 | 反应形成的新结构 | 反应类型 |
Ⅰ | $ {\rm {\mathrm{B}\mathrm{r}}_{2}} $ 的 $ {\rm {\mathrm{C}\mathrm{C}\mathrm{l}}_{4}} $ 溶液 | | 加成反应 |
Ⅱ | | $ {\rm {\mathrm{C}\mathrm{H}}_{2}\xlongequal{}{\mathrm{C}\mathrm{H}\mathrm{C}\mathrm{H}}_{2}{\mathrm{O}\mathrm{O}\mathrm{C}\mathrm{C}\mathrm{H}}_{3}} $ | |
(3) 反应①的化学方程式为 。
(4) 反应③的化学方程式为 。
(5) 下列说法正确的有 (填序号)。
A. A中所有原子共平面
B. B和乙醇互为同系物
C. $ {\rm \mathrm{F}} $ 易溶于水,可作食品添加剂
D. 氢氧化铜能鉴别B、D两种无色液体
(6) 与B含有相同官能团的B的同分异构体的结构简式为 。
答案:(1) $ {\rm {\mathrm{H}}_{2}} $ ;羧基
(2) $ {\rm {\mathrm{C}\mathrm{H}}_{2}{\mathrm{B}\mathrm{r}\mathrm{C}\mathrm{H}\mathrm{B}\mathrm{r}\mathrm{C}\mathrm{H}}_{2}\mathrm{O}\mathrm{H}} $ ; $ {\rm {\mathrm{C}\mathrm{H}}_{3}\mathrm{C}\mathrm{O}\mathrm{O}\mathrm{H}} $ 、浓硫酸;取代(或酯化)反应
(3) 
(4) $ {\rm 2{\mathrm{C}\mathrm{H}}_{3}{\mathrm{C}\mathrm{H}}_{2}{\mathrm{C}\mathrm{H}}_{2}\mathrm{O}\mathrm{H}+{\mathrm{O}}_{2}{\xrightarrow[ △]{\mathrm{C}\mathrm{u}}}2{\mathrm{C}\mathrm{H}}_{3}{\mathrm{C}\mathrm{H}}_{2}\mathrm{C}\mathrm{H}\mathrm{O}+2{\mathrm{H}}_{2}\mathrm{O}} $
(5) BD
(6) $ {\rm {\mathrm{C}\mathrm{H}}_{3}\mathrm{C}\mathrm{H}(\mathrm{O}\mathrm{H}){\mathrm{C}\mathrm{H}}_{3}} $
解析:(1) 由分析知,物质 $ {\rm \mathrm{X}} $ 的化学式为 $ {\rm {\mathrm{H}}_{2}} $ , $ {\rm \mathrm{D}} $ 为 $ {\rm {\mathrm{C}\mathrm{H}}_{3}{\mathrm{C}\mathrm{H}}_{2}\mathrm{C}\mathrm{O}\mathrm{O}\mathrm{H}} $ ,官能团名称为羧基。
(2) $ {\rm \mathrm{A}} $ 中含有碳碳双键,可与 $ {\rm {\mathrm{B}\mathrm{r}}_{2}} $ 发生加成反应生成 $ {\rm {\mathrm{C}\mathrm{H}}_{2}{\mathrm{B}\mathrm{r}\mathrm{C}\mathrm{H}\mathrm{B}\mathrm{r}\mathrm{C}\mathrm{H}}_{2}\mathrm{O}\mathrm{H}} $ ;根据反应形成的新结构,可知其由 $ {\rm \mathrm{A}} $ 与 $ {\rm {\mathrm{C}\mathrm{H}}_{3}\mathrm{C}\mathrm{O}\mathrm{O}\mathrm{H}} $ 在浓硫酸加热条件下发生酯化反应得到,则反应试剂为 $ {\rm {\mathrm{C}\mathrm{H}}_{3}\mathrm{C}\mathrm{O}\mathrm{O}\mathrm{H}} $ 、浓硫酸,反应类型为取代(或酯化)反应。
(3) $ {\rm \mathrm{A}} $ 中碳碳双键断裂,发生加聚反应生成的 $ {\rm \mathrm{E}} $ 为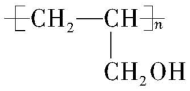 ,化学方程式为
,化学方程式为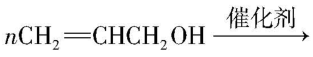
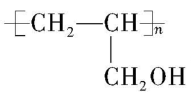 。
。
(4) 反应③为醇的催化氧化,化学方程式为 $ {\rm 2{\mathrm{C}\mathrm{H}}_{3}{\mathrm{C}\mathrm{H}}_{2}{\mathrm{C}\mathrm{H}}_{2}\mathrm{O}\mathrm{H}+{\mathrm{O}}_{2}{\xrightarrow[ △]{\mathrm{C}\mathrm{u}}}2{\mathrm{C}\mathrm{H}}_{3}{\mathrm{C}\mathrm{H}}_{2}\mathrm{C}\mathrm{H}\mathrm{O}+2{\mathrm{H}}_{2}\mathrm{O}} $ 。
(5) $ {\rm \mathrm{A}} $ 含有饱和碳原子,所有原子一定不能共平面, $ {\rm \mathrm{A}} $ 错误; $ {\rm \mathrm{B}} $ 为 $ {\rm {\mathrm{C}\mathrm{H}}_{3}{\mathrm{C}\mathrm{H}}_{2}{\mathrm{C}\mathrm{H}}_{2}\mathrm{O}\mathrm{H}} $ , $ {\rm \mathrm{B}} $ 和乙醇结构相似,分子组成相差1个 $ {\rm {\mathrm{C}\mathrm{H}}_{2}} $ 原子团,两者互为同系物, $ {\rm \mathrm{B}} $ 正确; $ {\rm \mathrm{F}} $ 为 $ {\rm {\mathrm{C}\mathrm{H}}_{3}{\mathrm{C}\mathrm{H}}_{2}{\mathrm{C}\mathrm{O}\mathrm{O}\mathrm{C}\mathrm{H}}_{2}{\mathrm{C}\mathrm{H}}_{2}{\mathrm{C}\mathrm{H}}_{3}} $ ,含酯基,不易溶于水, $ {\rm \mathrm{C}} $ 错误; $ {\rm \mathrm{B}} $ 为 $ {\rm {\mathrm{C}\mathrm{H}}_{3}{\mathrm{C}\mathrm{H}}_{2}{\mathrm{C}\mathrm{H}}_{2}\mathrm{O}\mathrm{H}} $ ,与 $ {\rm \mathrm{C}\mathrm{u}(\mathrm{O}\mathrm{H})_{2}} $ 不反应, $ {\rm \mathrm{D}} $ 为 $ {\rm {\mathrm{C}\mathrm{H}}_{3}{\mathrm{C}\mathrm{H}}_{2}\mathrm{C}\mathrm{O}\mathrm{O}\mathrm{H}} $ ,含有羧基,具有弱酸性,能与氢氧化铜反应生成 $ {\rm {\mathrm{C}\mathrm{u}}^{2+}} $ ,使氢氧化铜溶解得到蓝色溶液, $ {\rm \mathrm{C}\mathrm{u}(\mathrm{O}\mathrm{H})_{2}} $ 能鉴别 $ {\rm \mathrm{B}} $ 、 $ {\rm \mathrm{D}} $ 两种无色液体, $ {\rm \mathrm{D}} $ 正确。
(6) 与 $ {\rm \mathrm{B}({\mathrm{C}\mathrm{H}}_{3}{\mathrm{C}\mathrm{H}}_{2}{\mathrm{C}\mathrm{H}}_{2}\mathrm{O}\mathrm{H})} $ 含有相同官能团(羟基)的 $ {\rm \mathrm{B}} $ 的同分异构体的结构简式为 $ {\rm {\mathrm{C}\mathrm{H}}_{3}\mathrm{C}\mathrm{H}(\mathrm{O}\mathrm{H}){\mathrm{C}\mathrm{H}}_{3}} $ 。
11.餐厨垃圾在酶的作用下可转化为乙醇,进一步反应可制备有机物C和高分子材料 $ {\rm \mathrm{G}} $ ,转化关系如下:
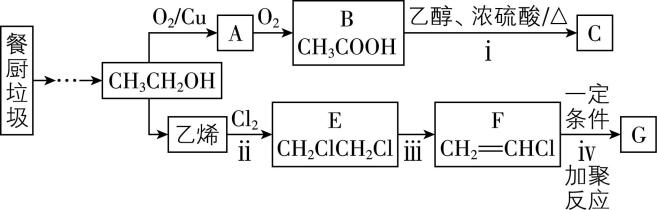
已知:有机化合物在一定条件下,从一个分子中脱去一个或 $ n $ 个小分子(如 $ {\rm {\mathrm{H}}_{2}\mathrm{O}} $ 、 $ {\rm \mathrm{H}\mathrm{X}} $ 等),生成含不饱和键的化合物的反应叫做消去反应,如ⅲ。
(1) B中含有的官能团名称是 。
(2) 反应ⅱ的反应类型是 。
(3) 反应ⅰ的化学方程式是 。
(4) $ {\rm \mathrm{G}} $ 的结构简式是 。
(5) 下列说法中,正确的是 (填序号)。
$ {\rm \mathrm{a}.\mathrm{E}} $ 、 $ {\rm \mathrm{F}} $ 均属于烃
$ {\rm \mathrm{b}.\mathrm{E}} $ 的同分异构体只有1种
$ {\rm \mathrm{c}.\mathrm{F}} $ 和 $ {\rm \mathrm{G}} $ 都能使酸性高锰酸钾溶液褪色
(6) 写出满足下列条件的一种结构简式: 。
①乙烯的同系物;②只有一种等效氢;③碳原子数小于等于10。
答案:(1) 羧基
(2) 加成反应
(3) $ {\rm {\mathrm{C}\mathrm{H}}_{3}\mathrm{C}\mathrm{O}\mathrm{O}\mathrm{H}+{\mathrm{C}\mathrm{H}}_{3}{\mathrm{C}\mathrm{H}}_{2}\mathrm{O}\mathrm{H}\stackrel{浓硫酸}{\underset{△}{⇌}}{\mathrm{C}\mathrm{H}}_{3}{\mathrm{C}\mathrm{O}\mathrm{O}\mathrm{C}\mathrm{H}}_{2}{\mathrm{C}\mathrm{H}}_{3}+{\mathrm{H}}_{2}\mathrm{O}} $
(4) 
(5) $ \mathrm{b} $
(6) 
解析:(1) $ {\rm \mathrm{B}} $ 是 $ {\rm {\mathrm{C}\mathrm{H}}_{3}\mathrm{C}\mathrm{O}\mathrm{O}\mathrm{H}} $ ,含有的官能团是羧基。
(2) 反应ⅱ为乙烯和氯气发生的加成反应。
(3) 反应ⅰ为乙酸和乙醇发生酯化反应生成乙酸乙酯和水,化学方程式是 $ {\rm {\mathrm{C}\mathrm{H}}_{3}\mathrm{C}\mathrm{O}\mathrm{O}\mathrm{H}+{\mathrm{C}\mathrm{H}}_{3}{\mathrm{C}\mathrm{H}}_{2}\mathrm{O}\mathrm{H}\stackrel{浓硫酸}{\underset{△}{⇌}}{\mathrm{C}\mathrm{H}}_{3}{\mathrm{C}\mathrm{O}\mathrm{O}\mathrm{C}\mathrm{H}}_{2}{\mathrm{C}\mathrm{H}}_{3}+{\mathrm{H}}_{2}\mathrm{O}} $ 。
(4) $ {\rm \mathrm{G}} $ 为聚氯乙烯,结构简式是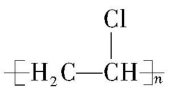 。
。
(5) 烃是指由碳和氢两种元素组成的有机化合物, $ {\rm \mathrm{E}} $ 、 $ {\rm \mathrm{F}} $ 中均含氯元素, $ \mathrm{a} $ 错误; $ {\rm \mathrm{E}} $ 的同分异构体只有 $ {\rm {\mathrm{C}\mathrm{H}\mathrm{C}\mathrm{l}}_{2}{\mathrm{C}\mathrm{H}}_{3}} $ , $ \mathrm{b} $ 正确; $ {\rm \mathrm{G}} $ 中不含碳碳双键,不能使酸性高锰酸钾溶液褪色, $ \mathrm{c} $ 错误。
(6) ①乙烯的同系物只有一个碳碳双键,②只有一种等效氢,③碳原子数小于等于10,则满足条件的结构是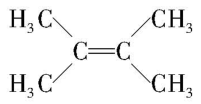 。
。
12.烯烃在有机合成中有重要作用,其反应机理及制备是化学研究的热点。回答下列问题。
Ⅰ.乙烯催化氧化的过程如图甲所示(部分相关离子未画出):
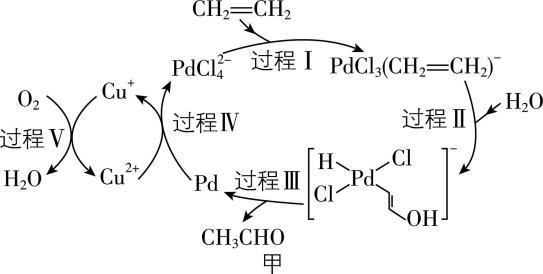
(1) 该过程中 $ {\rm {\mathrm{C}\mathrm{u}}^{+}} $ 的作用是 ,乙烯催化氧化反应的化学方程式为 。
Ⅱ.实验室用乙醇制备乙烯原理如下: $ {\rm {\mathrm{C}\mathrm{H}}_{3}{\mathrm{C}\mathrm{H}}_{2}\mathrm{O}\mathrm{H}{\xrightarrow[ ~170℃]{浓硫酸}}{\mathrm{C}\mathrm{H}}_{2}\stackrel{}{=}{\mathrm{C}\mathrm{H}}_{2}↑+{\mathrm{H}}_{2}\mathrm{O}} $ ,部分实验装置见图乙。
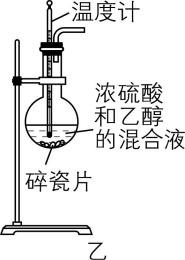
(2) 下列关于该实验的说法正确的是 (填序号)。
A. 碎瓷片可防止溶液暴沸
B. 应将浓硫酸缓慢加入乙醇中
C. 水浴加热能满足实验所需条件
(3) 用浓硫酸作催化剂时,若加热温度过高,在圆底烧瓶中会产生黑色物质 (填物质名称或化学式),进而发生副反应,产生 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 、 $ {\rm {\mathrm{C}\mathrm{O}}_{2}} $ 气体。为证明乙烯中混有 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ ,可选用 (填序号)。
A.稀硫酸B. $ {\rm \mathrm{N}\mathrm{a}\mathrm{O}\mathrm{H}} $ 溶液
C.酸性 $ {\rm {\mathrm{K}\mathrm{M}\mathrm{n}\mathrm{O}}_{4}} $ 溶液D.品红溶液
(4) 甲同学将初步净化的乙烯(除去 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 、 $ {\rm {\mathrm{C}\mathrm{O}}_{2}} $ )通入溴的四氯化碳溶液中,溶液完全褪色需要约 $ 4 \min $ ;乙同学将未干燥气体通入同浓度的四氯化碳溶液中,溶液完全褪色需要约 $ 2 \min $ 。原因分析:烯烃与溴反应过程的机理如图丙所示,
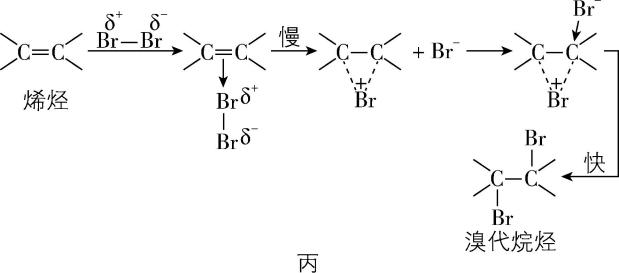
反应物正电性部分与双键反应步骤进行得较慢,带负电粒子与正离子反应步骤进行得较快。 $ {\rm {\mathrm{B}\mathrm{r}}_{2}} $ 与水反应生成的 $ {\rm \mathrm{H}\mathrm{B}\mathrm{r}\mathrm{O}} $ (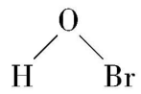 )中的 $ {\rm \mathrm{B}\mathrm{r}} $ 正电性强于 $ {\rm {\mathrm{B}\mathrm{r}}_{2}} $ 中的 $ {\rm \mathrm{B}\mathrm{r}} $ ,故乙同学的实验速率快。由此机理可知,乙烯通入溴水,除溴代烷烃外,还可能会生成有机产物 (写结构简式)。
)中的 $ {\rm \mathrm{B}\mathrm{r}} $ 正电性强于 $ {\rm {\mathrm{B}\mathrm{r}}_{2}} $ 中的 $ {\rm \mathrm{B}\mathrm{r}} $ ,故乙同学的实验速率快。由此机理可知,乙烯通入溴水,除溴代烷烃外,还可能会生成有机产物 (写结构简式)。
答案:(1) 催化剂; $ {\rm 2{\mathrm{C}\mathrm{H}}_{2}\xlongequal{}{\mathrm{C}\mathrm{H}}_{2}+{\mathrm{O}}_{2}{\xrightarrow[ ~]{催化剂}}2{\mathrm{C}\mathrm{H}}_{3}\mathrm{C}\mathrm{H}\mathrm{O}} $
(2) AB
(3) C(或碳);D
(4) $ {\rm {\mathrm{C}\mathrm{H}}_{2}{\mathrm{O}\mathrm{H}\mathrm{C}\mathrm{H}}_{2}\mathrm{B}\mathrm{r}} $
解析:(1) 从反应机理图看, $ {\rm {\mathrm{C}\mathrm{u}}^{+}} $ 在过程Ⅴ中参与反应,又在过程Ⅳ中生成,为反应的催化剂;分析反应机理图知,乙烯、氧气是总反应的反应物,乙醛为总反应的生成物,结合原子守恒,可知乙烯催化氧化反应的化学方程式为 $ {\rm 2{\mathrm{C}\mathrm{H}}_{2}\xlongequal{}{\mathrm{C}\mathrm{H}}_{2}+{\mathrm{O}}_{2}{\xrightarrow[ ~]{催化剂}}2{\mathrm{C}\mathrm{H}}_{3}\mathrm{C}\mathrm{H}\mathrm{O}} $ 。
(2) 加热时,碎瓷片成为液体的汽化中心,让气泡有序形成、释放,可以防止液体暴沸, $ {\rm \mathrm{A}} $ 正确;将浓硫酸缓慢加入乙醇中,可以避免由于浓硫酸的稀释放热而引起的局部过热、酸液飞溅的危险, $ {\rm \mathrm{B}} $ 正确;通常状况下水的沸点是 $ 100℃ $ ,本实验所需反应温度为 $ 170℃ $ ,水浴加热达不到实验条件, $ {\rm \mathrm{C}} $ 错误。
(3) 用浓硫酸作催化剂时,若加热温度过高,浓硫酸能使部分乙醇脱水炭化,在圆底烧瓶中会产生黑色物质 $ {\rm \mathrm{C}} $ (或碳), $ {\rm \mathrm{C}} $ 可与浓硫酸发生反应产生 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 、 $ {\rm {\mathrm{C}\mathrm{O}}_{2}} $ 气体。 $ {\rm {\mathrm{C}\mathrm{O}}_{2}} $ 、 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 、乙烯均不与稀硫酸反应,不能用稀硫酸检验 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ ;乙烯不与氢氧化钠反应, $ {\rm {\mathrm{C}\mathrm{O}}_{2}} $ 、二氧化硫与氢氧化钠反应无明显现象,不可选用 $ {\rm \mathrm{N}\mathrm{a}\mathrm{O}\mathrm{H}} $ 溶液;乙烯、二氧化硫均能使酸性高锰酸钾溶液褪色,不可选用酸性 $ {\rm {\mathrm{K}\mathrm{M}\mathrm{n}\mathrm{O}}_{4}} $ 溶液; $ {\rm {\mathrm{C}\mathrm{O}}_{2}} $ 、乙烯与品红溶液均不反应,二氧化硫具有漂白性,能使品红溶液褪色,品红溶液可检验 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ ,故选 $ {\rm \mathrm{D}} $ 。
(4) 溴水中存在反应: $ {\rm {\mathrm{B}\mathrm{r}}_{2}+{\mathrm{H}}_{2}\mathrm{O}⇌\mathrm{H}\mathrm{B}\mathrm{r}+\mathrm{H}\mathrm{B}\mathrm{r}\mathrm{O}} $ ,由于 $ {\rm \mathrm{H}\mathrm{B}\mathrm{r}\mathrm{O}} $ (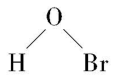 )中的 $ {\rm \mathrm{B}\mathrm{r}} $ 正电性强于 $ {\rm {\mathrm{B}\mathrm{r}}_{2}} $ 中的 $ {\rm \mathrm{B}\mathrm{r}} $ ,乙烯还可能与 $ {\rm \mathrm{H}\mathrm{B}\mathrm{r}\mathrm{O}} $ 发生加成反应生成 $ {\rm {\mathrm{C}\mathrm{H}}_{2}{\mathrm{O}\mathrm{H}\mathrm{C}\mathrm{H}}_{2}\mathrm{B}\mathrm{r}} $ ,反应方程式为 $ {\rm {\mathrm{C}\mathrm{H}}_{2}\xlongequal{}{\mathrm{C}\mathrm{H}}_{2}+\mathrm{H}—\mathrm{O}—\mathrm{B}\mathrm{r}\to {\mathrm{C}\mathrm{H}}_{2}{\mathrm{O}\mathrm{H}\mathrm{C}\mathrm{H}}_{2}\mathrm{B}\mathrm{r}} $ 。
)中的 $ {\rm \mathrm{B}\mathrm{r}} $ 正电性强于 $ {\rm {\mathrm{B}\mathrm{r}}_{2}} $ 中的 $ {\rm \mathrm{B}\mathrm{r}} $ ,乙烯还可能与 $ {\rm \mathrm{H}\mathrm{B}\mathrm{r}\mathrm{O}} $ 发生加成反应生成 $ {\rm {\mathrm{C}\mathrm{H}}_{2}{\mathrm{O}\mathrm{H}\mathrm{C}\mathrm{H}}_{2}\mathrm{B}\mathrm{r}} $ ,反应方程式为 $ {\rm {\mathrm{C}\mathrm{H}}_{2}\xlongequal{}{\mathrm{C}\mathrm{H}}_{2}+\mathrm{H}—\mathrm{O}—\mathrm{B}\mathrm{r}\to {\mathrm{C}\mathrm{H}}_{2}{\mathrm{O}\mathrm{H}\mathrm{C}\mathrm{H}}_{2}\mathrm{B}\mathrm{r}} $ 。

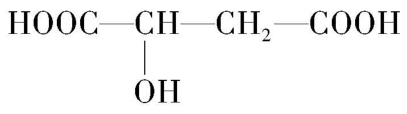 。下列相关说法不正确的是( )
。下列相关说法不正确的是( )
 。下列说法不正确的是( )
。下列说法不正确的是( ) 和苯乙炔不互为同系物
和苯乙炔不互为同系物 和 $ {\rm {\mathrm{C}\mathrm{H}}_{3}\mathrm{B}\mathrm{r}} $
和 $ {\rm {\mathrm{C}\mathrm{H}}_{3}\mathrm{B}\mathrm{r}} $  分子中含有两个碳碳三键,苯乙炔分子中只含有一个碳碳三键,二者结构不相似,不互为同系物, $ {\rm \mathrm{B}} $ 正确;高分子材料 $ {\rm \mathrm{P}} $ 中含有碳碳三键,能使溴的四氯化碳溶液褪色, $ {\rm \mathrm{C}} $ 正确;生成 $ {\rm \mathrm{P}} $ 的单体是
分子中含有两个碳碳三键,苯乙炔分子中只含有一个碳碳三键,二者结构不相似,不互为同系物, $ {\rm \mathrm{B}} $ 正确;高分子材料 $ {\rm \mathrm{P}} $ 中含有碳碳三键,能使溴的四氯化碳溶液褪色, $ {\rm \mathrm{C}} $ 正确;生成 $ {\rm \mathrm{P}} $ 的单体是 和 $ {\rm {\mathrm{C}\mathrm{H}}_{2}{\mathrm{B}\mathrm{r}}_{2}} $ , $ {\rm \mathrm{D}} $ 错误。
和 $ {\rm {\mathrm{C}\mathrm{H}}_{2}{\mathrm{B}\mathrm{r}}_{2}} $ , $ {\rm \mathrm{D}} $ 错误。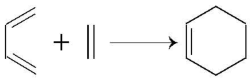 )取得重要进展。某 $ {\rm \mathrm{D}\mathrm{i}\mathrm{e}\mathrm{l}\mathrm{s}-\mathrm{A}\mathrm{l}\mathrm{d}\mathrm{e}\mathrm{r}} $ 反应由Ⅰ和Ⅲ反应生成Ⅴ的催化机理如图所示( $ {\rm —{\mathrm{C}\mathrm{O}}_{2}\mathrm{M}\mathrm{e}} $ 即 $ {\rm —{\mathrm{C}\mathrm{O}\mathrm{O}\mathrm{C}\mathrm{H}}_{3}} $ 、 $ {\rm —\mathrm{B}\mathrm{n}} $ 即
)取得重要进展。某 $ {\rm \mathrm{D}\mathrm{i}\mathrm{e}\mathrm{l}\mathrm{s}-\mathrm{A}\mathrm{l}\mathrm{d}\mathrm{e}\mathrm{r}} $ 反应由Ⅰ和Ⅲ反应生成Ⅴ的催化机理如图所示( $ {\rm —{\mathrm{C}\mathrm{O}}_{2}\mathrm{M}\mathrm{e}} $ 即 $ {\rm —{\mathrm{C}\mathrm{O}\mathrm{O}\mathrm{C}\mathrm{H}}_{3}} $ 、 $ {\rm —\mathrm{B}\mathrm{n}} $ 即 )。下列说法正确的是( )
)。下列说法正确的是( )
 结构不相似,分子组成上也不是相差若干个 $ {\rm {\mathrm{C}\mathrm{H}}_{2}} $ 原子团,两者不互为同系物, $ {\rm \mathrm{B}} $ 错误;由反应机理知, $ Ⅰ+Ⅵ\to Ⅹ+Ⅱ $ ,结合Ⅰ、Ⅵ、Ⅱ的结构简式可知, $ Ⅹ $ 为 $ {\rm {\mathrm{H}}_{2}\mathrm{O}} $ , $ {\rm \mathrm{C}} $ 正确;由催化机理可知,反应消耗了Ⅵ又生成了Ⅵ,Ⅵ是反应的催化剂,而Ⅳ在反应中先生成后又被消耗,是反应中间体, $ {\rm \mathrm{D}} $ 错误。
结构不相似,分子组成上也不是相差若干个 $ {\rm {\mathrm{C}\mathrm{H}}_{2}} $ 原子团,两者不互为同系物, $ {\rm \mathrm{B}} $ 错误;由反应机理知, $ Ⅰ+Ⅵ\to Ⅹ+Ⅱ $ ,结合Ⅰ、Ⅵ、Ⅱ的结构简式可知, $ Ⅹ $ 为 $ {\rm {\mathrm{H}}_{2}\mathrm{O}} $ , $ {\rm \mathrm{C}} $ 正确;由催化机理可知,反应消耗了Ⅵ又生成了Ⅵ,Ⅵ是反应的催化剂,而Ⅳ在反应中先生成后又被消耗,是反应中间体, $ {\rm \mathrm{D}} $ 错误。


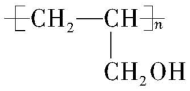 ,化学方程式为
,化学方程式为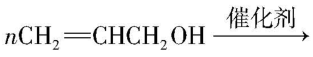
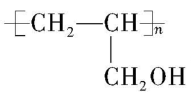 。
。


 。
。 。
。


 )中的 $ {\rm \mathrm{B}\mathrm{r}} $ 正电性强于 $ {\rm {\mathrm{B}\mathrm{r}}_{2}} $ 中的 $ {\rm \mathrm{B}\mathrm{r}} $ ,故乙同学的实验速率快。由此机理可知,乙烯通入溴水,除溴代烷烃外,还可能会生成有机产物 (写结构简式)。
)中的 $ {\rm \mathrm{B}\mathrm{r}} $ 正电性强于 $ {\rm {\mathrm{B}\mathrm{r}}_{2}} $ 中的 $ {\rm \mathrm{B}\mathrm{r}} $ ,故乙同学的实验速率快。由此机理可知,乙烯通入溴水,除溴代烷烃外,还可能会生成有机产物 (写结构简式)。 )中的 $ {\rm \mathrm{B}\mathrm{r}} $ 正电性强于 $ {\rm {\mathrm{B}\mathrm{r}}_{2}} $ 中的 $ {\rm \mathrm{B}\mathrm{r}} $ ,乙烯还可能与 $ {\rm \mathrm{H}\mathrm{B}\mathrm{r}\mathrm{O}} $ 发生加成反应生成 $ {\rm {\mathrm{C}\mathrm{H}}_{2}{\mathrm{O}\mathrm{H}\mathrm{C}\mathrm{H}}_{2}\mathrm{B}\mathrm{r}} $ ,反应方程式为 $ {\rm {\mathrm{C}\mathrm{H}}_{2}\xlongequal{}{\mathrm{C}\mathrm{H}}_{2}+\mathrm{H}—\mathrm{O}—\mathrm{B}\mathrm{r}\to {\mathrm{C}\mathrm{H}}_{2}{\mathrm{O}\mathrm{H}\mathrm{C}\mathrm{H}}_{2}\mathrm{B}\mathrm{r}} $ 。
)中的 $ {\rm \mathrm{B}\mathrm{r}} $ 正电性强于 $ {\rm {\mathrm{B}\mathrm{r}}_{2}} $ 中的 $ {\rm \mathrm{B}\mathrm{r}} $ ,乙烯还可能与 $ {\rm \mathrm{H}\mathrm{B}\mathrm{r}\mathrm{O}} $ 发生加成反应生成 $ {\rm {\mathrm{C}\mathrm{H}}_{2}{\mathrm{O}\mathrm{H}\mathrm{C}\mathrm{H}}_{2}\mathrm{B}\mathrm{r}} $ ,反应方程式为 $ {\rm {\mathrm{C}\mathrm{H}}_{2}\xlongequal{}{\mathrm{C}\mathrm{H}}_{2}+\mathrm{H}—\mathrm{O}—\mathrm{B}\mathrm{r}\to {\mathrm{C}\mathrm{H}}_{2}{\mathrm{O}\mathrm{H}\mathrm{C}\mathrm{H}}_{2}\mathrm{B}\mathrm{r}} $ 。