课时1 乙醇
一、刷基础
1.莽草酸可用于合成药物达菲,其结构简式如图所示,下列关于莽草酸的说法正确的是( )
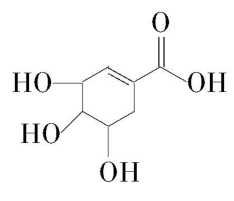
A. 分子式为 $ {\rm {\mathrm{C}}_{7}{\mathrm{H}}_{6}{\mathrm{O}}_{5}} $
B. 分子中含有四种官能团
C. 可发生加成和取代反应
D. 该有机物属于烃
答案:C
解析:根据结构简式可知,分子式为 $ {\rm {\mathrm{C}}_{7}{\mathrm{H}}_{10}{\mathrm{O}}_{5}} $ , $ {\rm \mathrm{A}} $ 错误;分子中含有羟基、羧基、碳碳双键,共三种官能团, $ {\rm \mathrm{B}} $ 错误;该分子中含碳碳双键,能发生加成反应,含羟基、羧基,能发生取代反应, $ {\rm \mathrm{C}} $ 正确;烃为仅含 $ {\rm \mathrm{C}} $ 、 $ {\rm \mathrm{H}} $ 元素的有机化合物,该分子中含 $ {\rm \mathrm{O}} $ 元素,不属于烃, $ {\rm \mathrm{D}} $ 错误。
2.下列反应与有机化合物中官能团的性质有关的是( )
A. 乙醇在空气中燃烧
B. 环己烷难溶于水
C. 乙烯使酸性高锰酸钾溶液褪色
D. 光照条件下,甲烷与氯气发生取代反应生成一氯甲烷等物质
答案:C
解析:乙醇的官能团为羟基,但乙醇在空气中燃烧与羟基的性质无关, $ {\rm \mathrm{A}} $ 错误;环己烷中不含官能团,即其难溶于水与官能团的性质无关, $ {\rm \mathrm{B}} $ 错误;乙烯分子中含有碳碳双键,导致其性质较活泼,能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,即该反应与乙烯中官能团的性质有关, $ {\rm \mathrm{C}} $ 正确;甲烷分子中没有官能团,即其与氯气在光照条件下发生取代反应生成一氯甲烷等物质与官能团的性质无关, $ {\rm \mathrm{D}} $ 错误。
3.下列和乙醇相关的化学用语表达正确的是( )
A. 乙醇分子中甲基的电子式为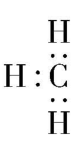
B. 乙醇的结构简式为 $ {\rm {\mathrm{C}}_{2}{\mathrm{H}}_{6}\mathrm{O}} $
C. 乙醇分子中羟基的电子式为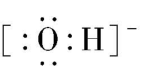
D. 乙醇分子的空间填充模型为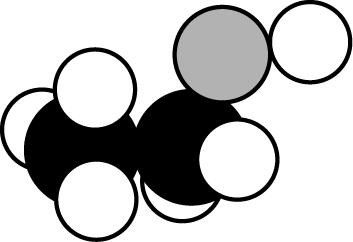
答案:D
解析:乙醇分子中含有甲基,甲基的结构简式为 $ {\rm —{\mathrm{C}\mathrm{H}}_{3}} $ ,其电子式为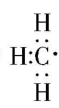 , $ {\rm \mathrm{A}} $ 错误;乙醇的结构简式为 $ {\rm {\mathrm{C}\mathrm{H}}_{3}{\mathrm{C}\mathrm{H}}_{2}\mathrm{O}\mathrm{H}} $ , $ {\rm \mathrm{B}} $ 错误;乙醇的官能团为羟基,羟基的结构简式为 $ {\rm —\mathrm{O}\mathrm{H}} $ ,其电子式为
, $ {\rm \mathrm{A}} $ 错误;乙醇的结构简式为 $ {\rm {\mathrm{C}\mathrm{H}}_{3}{\mathrm{C}\mathrm{H}}_{2}\mathrm{O}\mathrm{H}} $ , $ {\rm \mathrm{B}} $ 错误;乙醇的官能团为羟基,羟基的结构简式为 $ {\rm —\mathrm{O}\mathrm{H}} $ ,其电子式为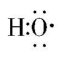 , $ {\rm \mathrm{C}} $ 错误;根据乙醇的结构式及 $ {\rm \mathrm{C}} $ 、 $ {\rm \mathrm{H}} $ 、 $ {\rm \mathrm{O}} $ 原子半径判断相对大小,题中所示乙醇的空间填充模型正确, $ {\rm \mathrm{D}} $ 正确。
, $ {\rm \mathrm{C}} $ 错误;根据乙醇的结构式及 $ {\rm \mathrm{C}} $ 、 $ {\rm \mathrm{H}} $ 、 $ {\rm \mathrm{O}} $ 原子半径判断相对大小,题中所示乙醇的空间填充模型正确, $ {\rm \mathrm{D}} $ 正确。
4.比较乙烷和乙醇的结构,下列说法错误的是( )
A. 分子中的化学键都包括极性键和非极性键
B. 分子中都含6个氢原子且6个氢原子的化学环境完全相同
C. 乙基与1个氢原子相连就是乙烷分子
D. 乙基与1个羟基相连就是乙醇分子
答案:B
解析:乙烷和乙醇分子中均包括极性键 $ {\rm (\mathrm{C}—\mathrm{H})} $ 和非极性键 $ {\rm (\mathrm{C}—\mathrm{C})} $ , $ {\rm \mathrm{A}} $ 正确;乙烷分子中6个氢原子等效,乙醇分子中含3种等效氢, $ {\rm \mathrm{B}} $ 错误;根据乙烷结构简式 $ {\rm ({\mathrm{C}\mathrm{H}}_{3}{\mathrm{C}\mathrm{H}}_{3})} $ 可知,乙基与1个氢原子相连就是乙烷分子, $ {\rm \mathrm{C}} $ 正确;根据乙醇结构简式 $ {\rm ({\mathrm{C}\mathrm{H}}_{3}{\mathrm{C}\mathrm{H}}_{2}\mathrm{O}\mathrm{H})} $ 可知,乙基与1个羟基相连就是乙醇分子, $ {\rm \mathrm{D}} $ 正确。
5.交警检验机动车驾驶员是否“酒驾”时,对驾驶员进行呼气酒精检测,一种传统的酒精检测仪原理:橙红色的重铬酸钾 $ {\rm [{\mathrm{K}}_{2}{\mathrm{C}\mathrm{r}}_{2}{\mathrm{O}}_{7}]} $ 与乙醇反应生成绿色的硫酸铬 $ {\rm [{\mathrm{C}\mathrm{r}}_{2} ({\mathrm{S}\mathrm{O}}_{4})_{3} ]} $ ,根据是否变色及颜色的变化程度,可测出呼出气体中是否有乙醇及含量高低。下列对乙醇的描述与此原理无关的是( )
①乙醇易挥发 ②乙醇密度比水小
③乙醇有还原性 ④乙醇是烃的含氧衍生物
A. ①③
B. ②③
C. ①④
D. ②④
答案:D
解析:检测原理:乙醇因具有还原性而能与酸性重铬酸钾溶液发生氧化还原反应,同时乙醇易挥发,会进入呼出气体中,因此能被检测,故选 $ {\rm \mathrm{D}} $ 。
6.下列关于乙醇结构与性质的说法正确的是( )
A. 乙醇分子中含有 $ {\rm —\mathrm{O}\mathrm{H}} $ ,所以乙醇可溶于水,也可电离出 $ {\rm {\mathrm{O}\mathrm{H}}^{-}} $
B. 乙醇能电离出 $ {\rm {\mathrm{H}}^{+}} $ ,所以是电解质
C. 乙醇与钠反应可以产生氢气,所以乙醇溶液显酸性
D. 向 $ 75\% $ 的酒精中加入钠,产生气泡,不能证明乙醇含有羟基
答案:D
解析:乙醇结构中含有 $ {\rm —\mathrm{O}\mathrm{H}} $ ,能与水形成氢键,所以乙醇可溶于水,但是不能电离出 $ {\rm {\mathrm{O}\mathrm{H}}^{-}} $ , $ {\rm \mathrm{A}} $ 错误;乙醇和钠反应可以产生氢气,但乙醇是非电解质,不能电离出氢离子,乙醇溶液不显酸性, $ {\rm \mathrm{B}} $ 、 $ {\rm \mathrm{C}} $ 错误; $ 75\% $ 酒精中含有水,水也可以与钠反应产生气泡,干扰实验, $ {\rm \mathrm{D}} $ 正确。
7.实验现象表明,乙醇与钠的反应比相同条件下水与钠的反应缓和得多。下列说法不正确的是( )
A. 在与钠反应的过程中,乙醇分子和水分子均发生了氢氧键的断裂
B. 将钠投入无水乙醇中,钠会沉入液体底部,说明乙醇的密度比水的小
C. 乙醇与钠的反应缓和得多,说明乙醇分子中羟基上的氢原子相对比较活泼
D. 若将质量相同的钠分别投入足量乙醇和水中,则产生的氢气的物质的量相同
答案:C
解析:乙醇分子与钠反应时断裂的是羟基中的氢氧键,水分子与钠反应时也断裂了氢氧键, $ {\rm \mathrm{A}} $ 正确;将钠投入无水乙醇中,钠会沉入液体底部,说明乙醇的密度比钠的小,而钠的密度小于水,则乙醇的密度比水的小, $ {\rm \mathrm{B}} $ 正确;乙醇与钠的反应缓和得多,则说明乙醇羟基中的氢原子相对不活泼, $ {\rm \mathrm{C}} $ 错误;若将质量相同的钠分别投入足量乙醇和水中,钠少量,钠能提供的电子数相同,则产生的氢气的物质的量相同, $ {\rm \mathrm{D}} $ 正确。
8.为了验证乙醇的结构式,利用乙醇和钠的反应,设计如图甲装置进行实验,在圆底烧瓶中放入足量的钠,从分液漏斗中缓缓滴入一定量的乙醇,通过测量量筒中水的体积,就可知反应生成的氢气的体积。
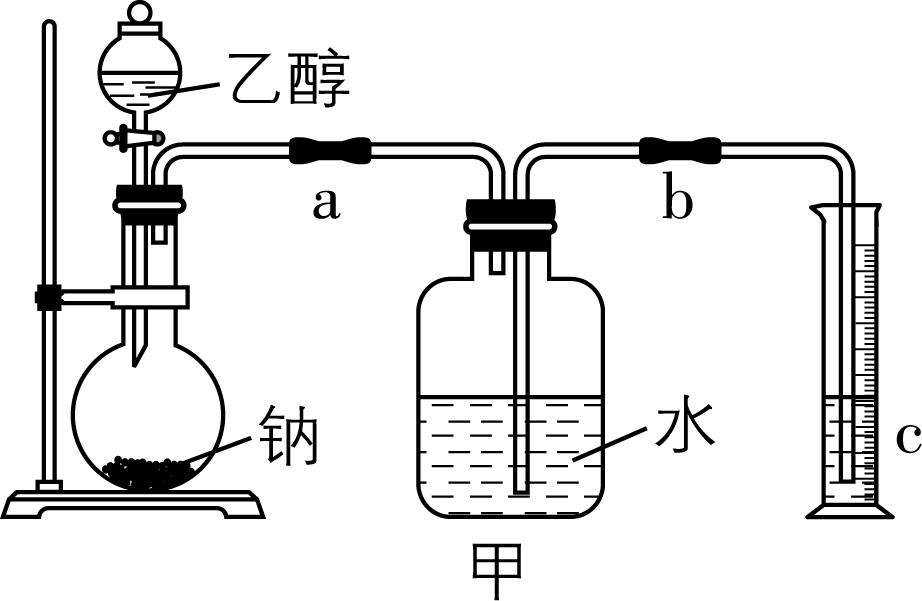
(1) 实验前检验该装置的气密性的实验操作是 。
(2) 有人认为装置中有空气,所测的气体体积应扣除装置中空气的体积,才是氢气的体积,你认为 (填“正确”或“不正确”)。
(3) 若实验中所用乙醇含有少量水则实验结果将 (填“偏大”或“偏小”,下同),若实验开始前 $ \mathrm{b} $ 导管内未充满水则实验结果将 。
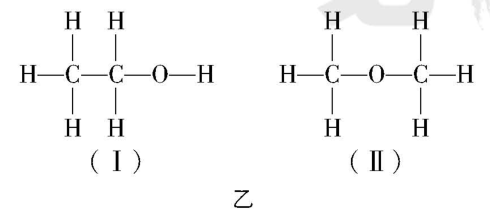
(4) 若测得有 $ {\rm 1.15\mathrm{g}{\mathrm{C}}_{2}{\mathrm{H}}_{6}\mathrm{O}} $ 参加反应,把量筒 $ \mathrm{c} $ 中的水的体积换算成标准状况下 $ {\rm {\mathrm{H}}_{2}} $ 的体积为 $ {\rm 280\mathrm{m}\mathrm{L}} $ ,试结合计算讨论有机化合物的结构为图乙中的 (填“Ⅰ”或“Ⅱ”)。
答案:(1) 连接好装置,关闭分液漏斗的活塞,将右侧导管插入水槽,微热烧瓶,若右侧导管口有气泡冒出,冷却后形成一段水柱,且一段时间内水柱液面不变,证明装置气密性良好
(2) 不正确
(3) 偏大;偏小
(4) Ⅰ(计算过程见解析)
解析:(1) 检查装置气密性时要先形成密闭体系,即先关闭分液漏斗活塞,把 $ \mathrm{c} $ 中导管插入液面下,然后手捂或微热烧瓶,使装置内外压强不同,具体操作见答案。
(2) 原来装置中有空气,但反应后装置中仍有空气,排出的气体的体积是装置中新生成的气态物质增加的体积,即氢气的体积,所以题中观点不正确。
(3) 等质量的水与钠反应产生氢气的量比乙醇与钠反应产生氢气的量多,如果乙醇中含有水,则导致实验结果偏大;如果实验开始前 $ \mathrm{b} $ 导管内未充满水,排到量筒中的水的体积偏小,则导致实验结果偏小。
(4) $ {\rm 1.15\mathrm{g}{\mathrm{C}}_{2}{\mathrm{H}}_{6}\mathrm{O}} $ 的物质的量为 $ \dfrac{1.15\mathrm{g}}{46\mathrm{g}\cdot {\mathrm{m}\mathrm{o}\mathrm{l}}^{-1}}=0.025\mathrm{m}\mathrm{o}\mathrm{l} $ ,生成氢气的物质的量为 $ {\rm \dfrac{0.28\mathrm{L}}{22.4\mathrm{L}\cdot {\mathrm{m}\mathrm{o}\mathrm{l}}^{-1}}=0.0125\mathrm{m}\mathrm{o}\mathrm{l}} $ ,即 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{C}}_{2}{\mathrm{H}}_{6}\mathrm{O}~0.5\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{H}}_{2}~1\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{H}} $ ,说明 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{C}}_{2}{\mathrm{H}}_{6}\mathrm{O}} $ 分子中有 $ 1\mathrm{m}\mathrm{o}\mathrm{l} $ 氢原子被钠置换,也就是说 $ {\rm {\mathrm{C}}_{2}{\mathrm{H}}_{6}\mathrm{O}} $ 分子中有1个氢原子与其他5个氢原子不同,其结构应为Ⅰ。
9.乙醇能发生如下反应:
$ {\rm {\textcircled{1}}{\mathrm{C}\mathrm{H}}_{3}{\mathrm{C}\mathrm{H}}_{2}\mathrm{O}\mathrm{H}+3{\mathrm{O}}_{2}{\xrightarrow[ ~]{点燃}}2{\mathrm{C}\mathrm{O}}_{2}+3{\mathrm{H}}_{2}\mathrm{O}} $ ;
$ {\rm ②2\mathrm{C}\mathrm{u}+{\mathrm{O}}_{2}\xlongequal{△}2\mathrm{C}\mathrm{u}\mathrm{O}} $ , $ {\rm {\mathrm{C}\mathrm{H}}_{3}{\mathrm{C}\mathrm{H}}_{2}\mathrm{O}\mathrm{H}+\mathrm{C}\mathrm{u}\mathrm{O}{\xrightarrow[ ~]{△}}{\mathrm{C}\mathrm{H}}_{3}\mathrm{C}\mathrm{H}\mathrm{O}+{\mathrm{H}}_{2}\mathrm{O}+\mathrm{C}\mathrm{u}} $ 。
由以上反应不能得出的结论是( )
A. 由反应①②可知,条件不同,乙醇与 $ {\rm {\mathrm{O}}_{2}} $ 反应的产物不同
B. 由反应②可知, $ {\rm \mathrm{C}\mathrm{u}} $ 是乙醇被氧化生成乙醛的催化剂
C. 由反应①可知,乙醇燃烧时,碳碳键、碳氢键均断裂
D. 由反应②可知,乙醇被氧化为乙醛时,只断裂氧氢键
答案:D
解析:由反应①可知,乙醇在氧气中燃烧生成 $ {\rm {\mathrm{C}\mathrm{O}}_{2}} $ 和 $ {\rm {\mathrm{H}}_{2}\mathrm{O}} $ ;由反应②可知,乙醇与 $ {\rm {\mathrm{O}}_{2}} $ 在铜作催化剂、加热的条件下,反应生成 $ {\rm {\mathrm{C}\mathrm{H}}_{3}\mathrm{C}\mathrm{H}\mathrm{O}} $ 和 $ {\rm {\mathrm{H}}_{2}\mathrm{O}} $ 。条件不同,乙醇与 $ {\rm {\mathrm{O}}_{2}} $ 反应生成的产物不同, $ {\rm \mathrm{A}} $ 正确。由反应②可知, $ {\rm \mathrm{C}\mathrm{u}} $ 在反应前后质量和化学性质不变,即铜作催化剂, $ {\rm \mathrm{B}} $ 正确。由反应①可知,乙醇燃烧时,碳碳键、碳氢键均断裂, $ {\rm \mathrm{C}} $ 正确。由反应②可知,乙醇被氧化为乙醛时,断裂了氧氢键、碳氢键, $ {\rm \mathrm{D}} $ 错误。
10.某小组同学探究不同条件下乙醇与氧化铜反应的产物,实验及结果如下所示。下列说法不正确的是( )
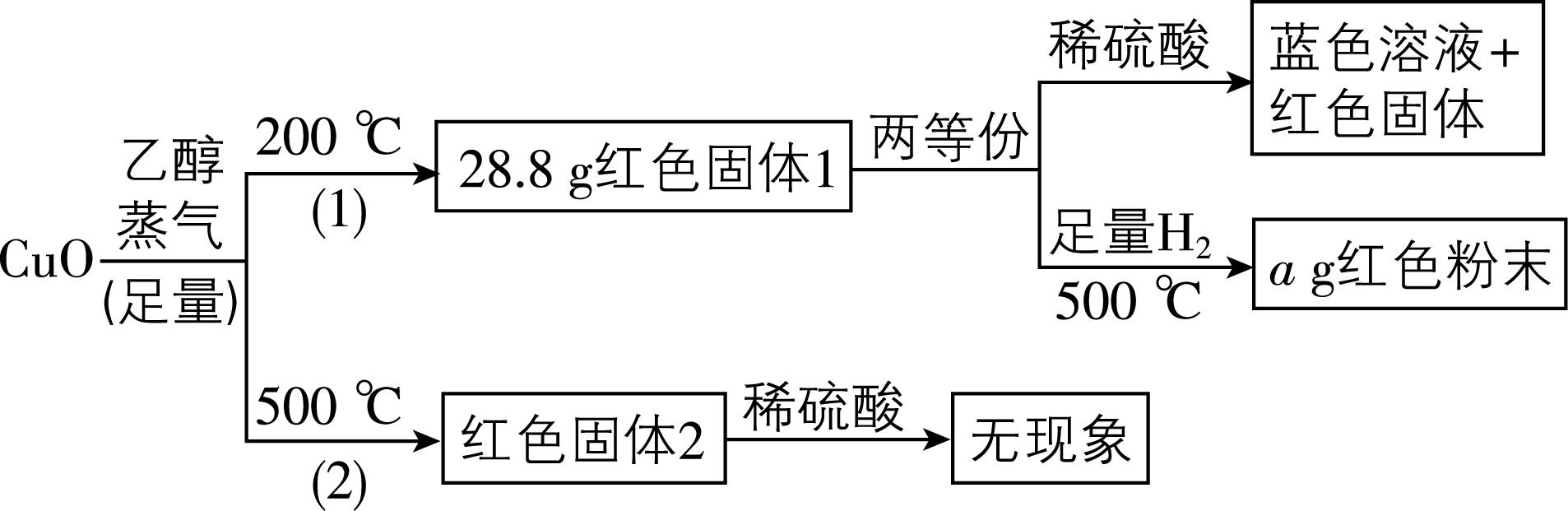
已知: $ {\rm {\mathrm{C}\mathrm{u}}_{2}\mathrm{O}} $ 为红色粉末状固体,几乎不溶于水,在酸性溶液中歧化为零价铜和二价铜。
A. 乙醇蒸气和 $ {\rm \mathrm{C}\mathrm{u}\mathrm{O}} $ 反应的产物与温度有关
B. 红色固体1中一定含有 $ {\rm {\mathrm{C}\mathrm{u}}_{2}\mathrm{O}} $ ,可能含有 $ {\rm \mathrm{C}\mathrm{u}} $
C. 若 $ a < 12.8 $ ,则红色固体1为 $ {\rm {\mathrm{C}\mathrm{u}}_{2}\mathrm{O}} $ 和 $ {\rm \mathrm{C}\mathrm{u}} $ 的混合物
D. 由实验可知: $ {\rm {\mathrm{C}}_{2}{\mathrm{H}}_{5}\mathrm{O}\mathrm{H}+\mathrm{C}\mathrm{u}\mathrm{O}{\xrightarrow[ ~]{500{℃}}}{\mathrm{C}\mathrm{H}}_{3}\mathrm{C}\mathrm{H}\mathrm{O}+\mathrm{C}\mathrm{u}+{\mathrm{H}}_{2}\mathrm{O}} $
答案:C
解析:红色固体1和稀硫酸反应,可知 $ 200℃ $ 时反应产物中含有 $ {\rm {\mathrm{C}\mathrm{u}}_{2}\mathrm{O}} $ ,红色固体2和稀硫酸不反应,则 $ 500℃ $ 时反应产物中只有 $ {\rm \mathrm{C}\mathrm{u}} $ ,说明乙醇蒸气和 $ {\rm \mathrm{C}\mathrm{u}\mathrm{O}} $ 反应的产物与温度有关, $ {\rm \mathrm{A}} $ 正确; $ {\rm {\mathrm{C}\mathrm{u}}_{2}\mathrm{O}} $ 在酸性溶液中歧化为零价铜和二价铜,红色固体1和稀硫酸反应得到蓝色溶液和红色固体,则红色固体1中一定含有 $ {\rm {\mathrm{C}\mathrm{u}}_{2}\mathrm{O}} $ ,可能含有 $ {\rm \mathrm{C}\mathrm{u}} $ , $ {\rm \mathrm{B}} $ 正确; $ {\rm 14.4\mathrm{g}{\mathrm{C}\mathrm{u}}_{2}\mathrm{O}} $ 被氢气还原生成 $ 12.8\mathrm{g} $ 铜,若红色固体1为 $ {\rm {\mathrm{C}\mathrm{u}}_{2}\mathrm{O}} $ 和 $ {\rm \mathrm{C}\mathrm{u}} $ 的混合物, $ a > 12.8 $ , $ {\rm \mathrm{C}} $ 错误;由实验可知 $ 500℃ $ 时反应产物中只有 $ {\rm \mathrm{C}\mathrm{u}} $ ,反应方程式为 $ {\rm {\mathrm{C}}_{2}{\mathrm{H}}_{5}\mathrm{O}\mathrm{H}+\mathrm{C}\mathrm{u}\mathrm{O}{\xrightarrow[ ~]{500{℃}}}{\mathrm{C}\mathrm{H}}_{3}\mathrm{C}\mathrm{H}\mathrm{O}+\mathrm{C}\mathrm{u}+{\mathrm{H}}_{2}\mathrm{O}} $ , $ {\rm \mathrm{D}} $ 正确。
11.实验室利用乙醇催化氧化制取粗乙醛的反应装置如图所示。下列说法错误的是( )
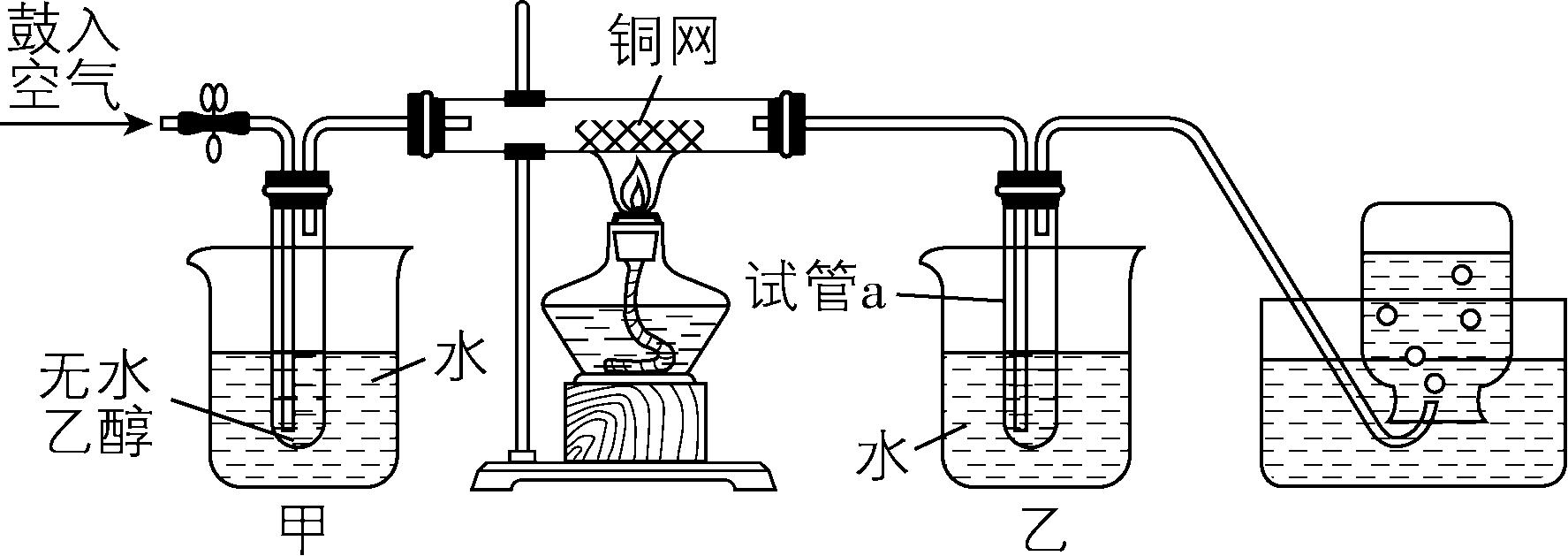
A. 该反应过程中涉及极性键的断裂和形成
B. 收集试管 $ \mathrm{a} $ 中的物质,加入 $ {\rm \mathrm{N}\mathrm{a}} $ 有可燃性气体生成,说明产物粗乙醛中混有乙醇
C. 该反应中铜为催化剂,硬质玻璃管中铜网出现红黑交替现象
D. 甲中选用热水,有利于乙醇挥发;乙中选用冷水,有利于冷凝收集产物
答案:B
解析:乙醇催化氧化制取粗乙醛的反应方程式为 $ {\rm 2{\mathrm{C}\mathrm{H}}_{3}{\mathrm{C}\mathrm{H}}_{2}\mathrm{O}\mathrm{H}+{\mathrm{O}}_{2}{\xrightarrow[ △]{\mathrm{C}\mathrm{u}}}2{\mathrm{C}\mathrm{H}}_{3}\mathrm{C}\mathrm{H}\mathrm{O}+2{\mathrm{H}}_{2}\mathrm{O}} $ ,该反应中有 $ {\rm \mathrm{C}—\mathrm{H}} $ 、 $ {\rm \mathrm{O}—\mathrm{H}} $ 极性键的断裂,也有 $ {\rm \mathrm{C}\xlongequal{}\mathrm{O}} $ 极性键的形成, $ {\rm \mathrm{A}} $ 正确;乙醇的催化氧化过程中有水生成,试管 $ \mathrm{a} $ 收集的产物含水, $ {\rm \mathrm{N}\mathrm{a}} $ 与水反应会产生可燃性气体 $ {\rm {\mathrm{H}}_{2}} $ 不能说明产物中混有乙醇, $ {\rm \mathrm{B}} $ 错误;该反应中铜为催化剂, $ {\rm \mathrm{C}\mathrm{u}} $ 首先被氧气氧化为 $ {\rm \mathrm{C}\mathrm{u}\mathrm{O}} $ ,之后 $ {\rm \mathrm{C}\mathrm{u}\mathrm{O}} $ 被乙醇重新还原为 $ {\rm \mathrm{C}\mathrm{u}} $ ,故硬质玻璃管中铜网会出现红黑交替现象, $ {\rm \mathrm{C}} $ 正确;装置甲需要把乙醇变为乙醇蒸气,则甲中的水为热水,装置乙用于收集乙醛,乙中的水为冷水,有利于冷凝收集乙醛, $ {\rm \mathrm{D}} $ 正确。





