第一节综合训练
一、刷能力
1.下列实验现象能充分说明发生了放热反应的是( )
选项 | A | B |
反应装置 | 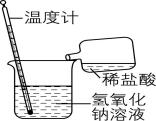
| 
|
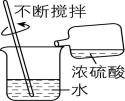
实验现象 | 温度计的水银柱不断上升 | 稀释时,烧杯壁温度明显升高 |
选项 | C | D |
反应装置 | 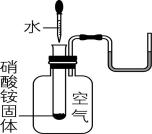
| 
|
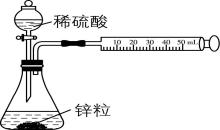
实验现象 | $ {\rm \mathrm{U}} $ 形管的液面左高右低 | 反应开始后,针筒活塞向右移动 |
解析:稀盐酸和氢氧化钠的反应为酸碱中和反应,温度计水银柱升高,说明发生放热反应, $ {\rm \mathrm{A}} $ 正确;浓硫酸稀释时放出大量热,但不是化学反应, $ {\rm \mathrm{B}} $ 错误;硝酸铵固体溶解吸热,使 $ {\rm \mathrm{U}} $ 形管液面出现左高右低的现象, $ {\rm \mathrm{C}} $ 错误;锌粒与稀硫酸反应产生氢气,不管反应是否放热,反应开始后,针筒活塞都向右移动, $ {\rm \mathrm{D}} $ 错误。
2.氮是动植物生长不可缺少的元素,氨的制备及应用对农业生产及国防建设均有重大意义。 $ {\rm {\mathrm{N}}_{2}} $ 和 $ {\rm {\mathrm{H}}_{2}} $ 在催化剂表面合成氨的微观历程及能量变化的示意图如图甲、乙所示。下列说法正确的是( )
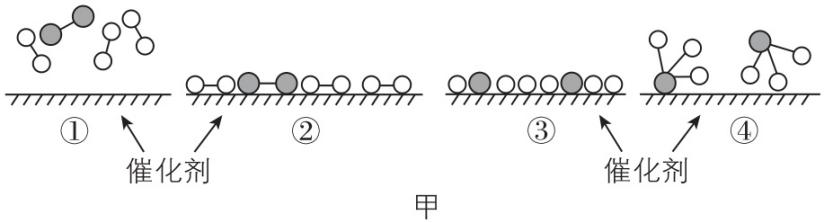
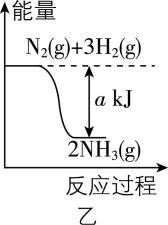
A. 将 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{N}}_{2}(\mathrm{g})} $ 和 $ {\rm 3\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{H}}_{2}(\mathrm{g})} $ 置于密闭容器中充分反应后,放出的热量等于 $ {\rm a\mathrm{k}\mathrm{J}} $
B. 该反应断开反应物中化学键吸收的总能量大于形成生成物中化学键释放的总能量
C. $ {\rm \mathrm{B}\mathrm{a}(\mathrm{O}\mathrm{H})_{2}\cdot 8{\mathrm{H}}_{2}\mathrm{O}} $ 晶体和 $ {\rm {\mathrm{N}\mathrm{H}}_{4}\mathrm{C}\mathrm{l}} $ 晶体反应的能量变化图也可以用图乙来表示
D. $ ③\to ④ $ 过程,是放热过程
答案:D
解析:合成氨反应是可逆反应,投入的 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{N}}_{2}(\mathrm{g})} $ 和 $ {\rm 3\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{H}}_{2}(\mathrm{g})} $ 不能完全反应,放出的热量小于 $ {\rm a\mathrm{k}\mathrm{J}} $ , $ {\rm \mathrm{A}} $ 错误;合成氨反应是放热反应,反应物断键吸收的能量小于生成物成键释放的能量, $ {\rm \mathrm{B}} $ 错误; $ {\rm \mathrm{B}\mathrm{a}(\mathrm{O}\mathrm{H})_{2}\cdot 8{\mathrm{H}}_{2}\mathrm{O}} $ 晶体和 $ {\rm {\mathrm{N}\mathrm{H}}_{4}\mathrm{C}\mathrm{l}} $ 晶体的反应是吸热反应,图乙是放热反应的能量变化图, $ {\rm \mathrm{C}} $ 错误; $ ③\to ④ $ 过程是成键过程,是放热过程, $ {\rm \mathrm{D}} $ 正确。
3.化学能可以与热能、电能等相互转化,下列说法正确的是( )
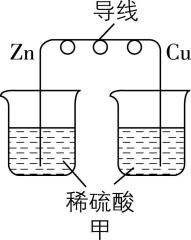
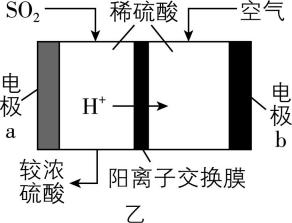
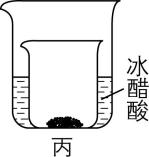
A. 图甲:能将化学能转化为电能
B. 图乙:电极 $ \mathrm{b} $ 为负极,发生氧化反应
C. 图乙:当电路中转移 $ 1\mathrm{m}\mathrm{o}\mathrm{l} $ 电子时,电极上消耗的 $ {\rm n({\mathrm{S}\mathrm{O}}_{2}):n({\mathrm{O}}_{2})=1:2} $
D. 图丙:小烧杯中盛有 $ {\rm {\mathrm{N}\mathrm{H}}_{4}\mathrm{C}\mathrm{l}} $ 晶体,向小烧杯中再加入适量氢氧化钡晶体 $ {\rm [\mathrm{B}\mathrm{a} (\mathrm{O}\mathrm{H})_{2}\cdot 8{\mathrm{H}}_{2}\mathrm{O} ]} $ ,搅拌,可观察到冰醋酸逐渐凝结为固体,证明小烧杯中的反应是吸热反应
答案:D
解析:图甲装置中,两个烧杯没用盐桥相连,没有形成闭合回路,不能构成原电池,所以不能将化学能转化为电能, $ {\rm \mathrm{A}} $ 错误。根据图乙中离子的流向可知,电极 $ \mathrm{a} $ 为负极,发生氧化反应;电极 $ \mathrm{b} $ 为正极,发生还原反应, $ {\rm \mathrm{B}} $ 错误。在图乙所示的原电池中, $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 在负极发生氧化反应: $ {\rm {\mathrm{S}\mathrm{O}}_{2}\sim 2{\mathrm{e}}^{-}\sim {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ , $ {\rm {\mathrm{O}}_{2}} $ 在正极发生还原反应: $ {\rm {\mathrm{O}}_{2}\sim 4{\mathrm{e}}^{-}\sim 2{\mathrm{H}}_{2}\mathrm{O}} $ ,根据得失电子守恒,当电路中转移 $ 1\mathrm{m}\mathrm{o}\mathrm{l} $ 电子时,电极上消耗的 $ {\rm n({\mathrm{S}\mathrm{O}}_{2}):n({\mathrm{O}}_{2})=2:1} $ , $ {\rm \mathrm{C}} $ 错误。向盛有 $ {\rm {\mathrm{N}\mathrm{H}}_{4}\mathrm{C}\mathrm{l}} $ 晶体的小烧杯中加入适量氢氧化钡晶体 $ {\rm [\mathrm{B}\mathrm{a} (\mathrm{O}\mathrm{H})_{2}\cdot 8{\mathrm{H}}_{2}\mathrm{O} ]} $ ,搅拌,观察到冰醋酸逐渐凝结为固体,说明大烧杯中的温度降低,即小烧杯中的反应吸收热量,是吸热反应, $ {\rm \mathrm{D}} $ 正确。
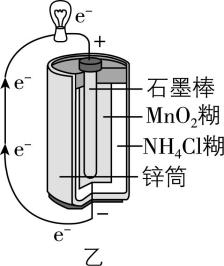
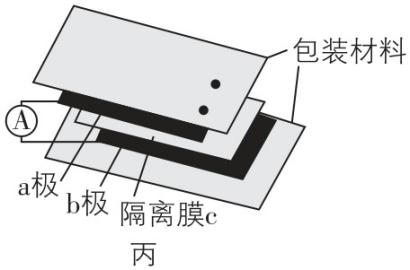
4.有关下列装置的说法不正确的是( )
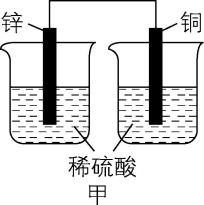
A. 图甲所示装置反应现象是,锌片溶解,锌片表面有气泡产生,铜片表面无明显现象
B. 图乙锌锰干电池属于一次电池,随着放电时间的增加,锌筒变薄
C. 图丙是“纸电池”,若 $ \mathrm{a} $ 极为铁、 $ \mathrm{b} $ 极为铜, $ \mathrm{c} $ 中含稀硝酸溶液时,铜为负极
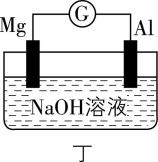
D. 图丁电池中 $ {\rm \mathrm{A}\mathrm{l}} $ 为负极,电极反应式为 $ {\rm \mathrm{A}\mathrm{l}-3{\mathrm{e}}^{-}+4{\mathrm{O}\mathrm{H}}^{-}\xlongequal{} [\mathrm{A}\mathrm{l} (\mathrm{O}\mathrm{H})_{4}{ ]}^{-}} $
答案:C
解析:图甲装置未形成闭合回路,不是原电池装置, $ {\rm \mathrm{Z}\mathrm{n}} $ 与稀硫酸反应产生氢气,锌片溶解,同时锌片表面有气泡产生,铜不与稀硫酸反应,无明显现象, $ {\rm \mathrm{A}} $ 正确;锌锰干电池属于一次电池, $ {\rm \mathrm{Z}\mathrm{n}} $ 作负极被氧化消耗,随着放电时间的增加,锌溶解,故锌筒变薄, $ {\rm \mathrm{B}} $ 正确;“纸电池”中,若 $ \mathrm{a} $ 极为铁、 $ \mathrm{b} $ 极为铜, $ \mathrm{c} $ 中含稀硝酸溶液,铁比铜活泼,则 $ {\rm \mathrm{F}\mathrm{e}} $ 为负极, $ {\rm \mathrm{C}} $ 错误;图丁电池中 $ {\rm \mathrm{M}\mathrm{g}} $ 虽然比 $ {\rm \mathrm{A}\mathrm{l}} $ 活泼,但 $ {\rm \mathrm{M}\mathrm{g}} $ 不与 $ {\rm \mathrm{N}\mathrm{a}\mathrm{O}\mathrm{H}} $ 溶液反应, $ {\rm \mathrm{A}\mathrm{l}} $ 为两性金属,可与 $ {\rm \mathrm{N}\mathrm{a}\mathrm{O}\mathrm{H}} $ 溶液反应,则由 $ {\rm \mathrm{M}\mathrm{g}} $ 、 $ {\rm \mathrm{A}\mathrm{l}} $ 和 $ {\rm \mathrm{N}\mathrm{a}\mathrm{O}\mathrm{H}} $ 溶液构成的原电池装置中, $ {\rm \mathrm{A}\mathrm{l}} $ 作负极发生氧化反应,电极反应式: $ {\rm \mathrm{A}\mathrm{l}-3{\mathrm{e}}^{-}+4{\mathrm{O}\mathrm{H}}^{-}\xlongequal{} [\mathrm{A}\mathrm{l} (\mathrm{O}\mathrm{H})_{4}{ ]}^{-}} $ , $ {\rm \mathrm{D}} $ 正确。
5.研究表明,在一定条件下,气态 $ {\rm \mathrm{H}\mathrm{C}\mathrm{N}} $ 转化为气态 $ {\rm \mathrm{C}\mathrm{N}\mathrm{H}} $ 的能量变化如图所示。下列说法正确的是( )
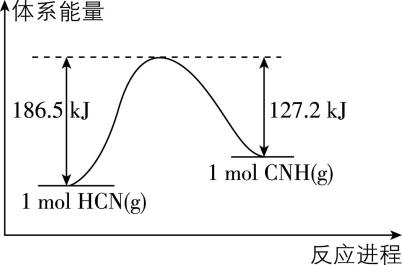
A. $ {\rm \mathrm{C}\mathrm{N}\mathrm{H}(\mathrm{g})} $ 比 $ {\rm \mathrm{H}\mathrm{C}\mathrm{N}(\mathrm{g})} $ 更稳定
B. $ {\rm \mathrm{H}\mathrm{C}\mathrm{N}(\mathrm{g})} $ 转化为 $ {\rm \mathrm{C}\mathrm{N}\mathrm{H}(\mathrm{g})} $ 一定要加热
C. 断开 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{H}\mathrm{C}\mathrm{N}(\mathrm{g})} $ 中所有的化学键需要放出 $ {\rm 127.2\mathrm{k}\mathrm{J}} $ 的能量
D. $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{H}\mathrm{C}\mathrm{N}(\mathrm{g})} $ 转化为 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{C}\mathrm{N}\mathrm{H}(\mathrm{g})} $ 需要吸收 $ {\rm 59.3\mathrm{k}\mathrm{J}} $ 的能量
答案:D
解析:物质的能量越低越稳定,根据题图可知,等物质的量的 $ {\rm \mathrm{H}\mathrm{C}\mathrm{N}(\mathrm{g})} $ 比 $ {\rm \mathrm{C}\mathrm{N}\mathrm{H}(\mathrm{g})} $ 的能量更低,因此 $ {\rm \mathrm{H}\mathrm{C}\mathrm{N}(\mathrm{g})} $ 比 $ {\rm \mathrm{C}\mathrm{N}\mathrm{H}(\mathrm{g})} $ 更稳定, $ {\rm \mathrm{A}} $ 错误;由题图可知, $ {\rm \mathrm{H}\mathrm{C}\mathrm{N}(\mathrm{g})\to \mathrm{C}\mathrm{N}\mathrm{H}(\mathrm{g})} $ 为吸热反应,但吸热反应不一定需要在加热条件下进行, $ {\rm \mathrm{B}} $ 错误;根据题图可知, $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{H}\mathrm{C}\mathrm{N}(\mathrm{g})} $ 转化为中间状态的物质需吸收 $ {\rm 186.5\mathrm{k}\mathrm{J}} $ 的能量,但由于该中间物质中可能仍然存在化学键,因此 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{H}\mathrm{C}\mathrm{N}(\mathrm{g})} $ 中的所有化学键全部断开需要吸收的能量大于或等于 $ {\rm 186.5\mathrm{k}\mathrm{J}} $ , $ {\rm \mathrm{C}} $ 错误;根据题图可知, $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{H}\mathrm{C}\mathrm{N}(\mathrm{g})} $ 转化为 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{C}\mathrm{N}\mathrm{H}(\mathrm{g})} $ 需要吸收的能量为 $ {\rm 186.5\mathrm{k}\mathrm{J}-127.2\mathrm{k}\mathrm{J}=59.3\mathrm{k}\mathrm{J}} $ , $ {\rm \mathrm{D}} $ 正确。
6.氢能驱动未来,某汽车氢氧燃料电池的结构简图如图,下列说法错误的是( )
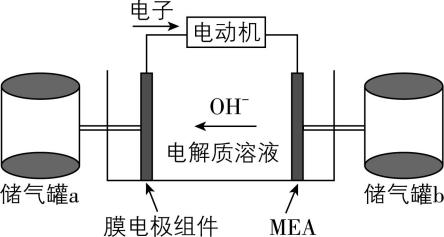
A. 储气罐 $ \mathrm{b} $ 中盛装的为氧气
B. 膜电极组件采用纳米材料可增大气体的吸收效率
C. 左侧电极发生的反应为 $ {\rm {\mathrm{H}}_{2}-2{\mathrm{e}}^{-}\xlongequal{}2{\mathrm{H}}^{+}} $
D. 一段时间后电解质溶液中 $ {\rm {\mathrm{O}\mathrm{H}}^{-}} $ 的浓度变小
答案:C
解析:由题图可知,电子沿导线自左至右移动,电解质溶液中 $ {\rm {\mathrm{O}\mathrm{H}}^{-}} $ 自右至左移动,可推测膜电极为负极,储气罐 $ \mathrm{a} $ 中气体为 $ {\rm {\mathrm{H}}_{2}} $ , $ {\rm \mathrm{M}\mathrm{E}\mathrm{A}} $ 电极为正极,储气罐 $ \mathrm{b} $ 中气体为 $ {\rm {\mathrm{O}}_{2}} $ 。储气罐 $ \mathrm{b} $ 盛装的气体为氧气, $ {\rm \mathrm{A}} $ 正确;纳米材料有较大的比表面积,可增大气体与膜电极接触面积,加快吸收效率, $ {\rm \mathrm{B}} $ 正确;膜电极为负极,电极反应式为 $ {\rm {\mathrm{H}}_{2}-2{\mathrm{e}}^{-}+2{\mathrm{O}\mathrm{H}}^{-}\xlongequal{}2{\mathrm{H}}_{2}\mathrm{O}} $ , $ {\rm \mathrm{C}} $ 错误;电池总反应为 $ {\rm 2{\mathrm{H}}_{2}+{\mathrm{O}}_{2}\xlongequal{}2{\mathrm{H}}_{2}\mathrm{O}} $ ,一段时间后溶剂水增多,电解质溶液浓度减小, $ {\rm \mathrm{D}} $ 正确。
7.科学家设计出质子膜 $ {\rm {\mathrm{H}}_{2}\mathrm{S}} $ 燃料电池,实现了利用 $ {\rm {\mathrm{H}}_{2}\mathrm{S}} $ 废气资源回收能量并得到单质硫。质子膜 $ {\rm {\mathrm{H}}_{2}\mathrm{S}} $ 燃料电池的结构示意图如图所示。下列说法不正确的是( )
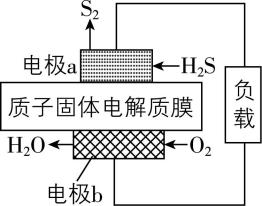
A. 电流方向:电极 $ \mathrm{b}\to $ 负载 $ \to $ 电极 $ \mathrm{a}\to $ 质子固体电解质膜 $ \to $ 电极 $ \mathrm{b} $
B. 电极 $ \mathrm{a} $ 上发生的电极反应为 $ {\rm 2{\mathrm{H}}_{2}\mathrm{S}-4{\mathrm{e}}^{-}\xlongequal{}{\mathrm{S}}_{2}+4{\mathrm{H}}^{+}} $
C. 每 $ {\rm 34\mathrm{g}{\mathrm{H}}_{2}\mathrm{S}} $ 参与反应,有 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{H}}^{+}} $ 经质子固体电解质膜进入正极区
D. 电路中每通过 $ 2\mathrm{m}\mathrm{o}\mathrm{l} $ 电子,在正极消耗 $ {\rm 11.2\mathrm{L}{\mathrm{O}}_{2}} $
答案:D
解析:电流由正极流向负极,即电流方向:电极 $ \mathrm{b}\to $ 负载 $ \to $ 电极 $ \mathrm{a}\to $ 质子固体电解质膜 $ \to $ 电极 $ \mathrm{b} $ , $ {\rm \mathrm{A}} $ 正确;根据思路导引可知, $ {\rm \mathrm{B}} $ 正确; $ {\rm 34\mathrm{g}{\mathrm{H}}_{2}\mathrm{S}} $ 物质的量 $ {\rm n({\mathrm{H}}_{2}\mathrm{S})=\dfrac{34\mathrm{g}}{34\mathrm{g}\cdot {\mathrm{m}\mathrm{o}\mathrm{l}}^{-1}}=1\mathrm{m}\mathrm{o}\mathrm{l}} $ ,根据负极反应式知,每 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{H}}_{2}\mathrm{S}} $ 参与反应,有 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{H}}^{+}} $ 经质子固体电解质膜进入正极区, $ {\rm \mathrm{C}} $ 正确;正极反应式为 $ {\rm {\mathrm{O}}_{2}+4{\mathrm{H}}^{+}+4{\mathrm{e}}^{-}\xlongequal{}2{\mathrm{H}}_{2}\mathrm{O}} $ ,电路中通过 $ 2\mathrm{m}\mathrm{o}\mathrm{l} $ 电子时,在正极消耗 $ {\rm 0.5\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{O}}_{2}} $ ,未指明标准状况,无法计算氧气的体积, $ {\rm \mathrm{D}} $ 错误。
8.常温下,将除去表面氧化膜的铝、铜片插入浓硝酸中组成原电池(如图甲所示),测得原电池的电流强度 $ {\rm (I)} $ 随时间 $ (t) $ 的变化如图乙所示,下列说法正确的是( )
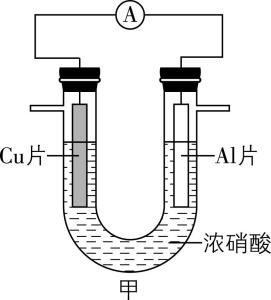
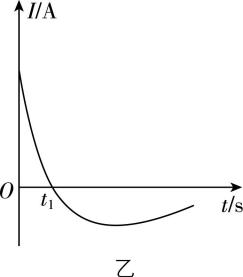
A. $ {\rm O ~} $ $ {t}_{1}\mathrm{s} $ ,原电池的负极是铜片
B. $ {\rm O ~} $ $ {t}_{1}\mathrm{s} $ ,正极发生还原反应,产生氢气
C. $ {t}_{1}\mathrm{s} $ 后,电流方向发生变化的原因是 $ {\rm \mathrm{A}\mathrm{l}} $ 在浓硝酸中发生钝化,氧化膜阻止了 $ {\rm \mathrm{A}\mathrm{l}} $ 进一步反应
D. $ {t}_{1}\mathrm{s} $ 后,电子从铝片流出经过外电路流向铜片
答案:C
解析:由题图可知,在 $ {t}_{1}\mathrm{s} $ 前后,电路中的电流方向是相反的。 $ {t}_{1}\mathrm{s} $ 前,因为铝比铜活泼,原电池的负极是铝片,铝发生氧化反应生成氧化铝,正极为铜; $ {t}_{1}\mathrm{s} $ 后,铝片表面生成的致密的氧化铝薄膜阻止了铝的进一步反应,负极变为铜片。根据上述分析可知, $ {\rm O} $ ~ $ {t}_{1}\mathrm{s} $ ,原电池的负极是铝片, $ {\rm \mathrm{A}} $ 错误;由分析可知, $ {\rm O} $ ~ $ {t}_{1}\mathrm{s} $ ,正极为铜,正极上硝酸根离子被还原为二氧化氮,正极的电极反应式为 $ {\rm 2{\mathrm{H}}^{+}+{\mathrm{N}\mathrm{O}}_{3}^{-}+{\mathrm{e}}^{-}\xlongequal{}{\mathrm{N}\mathrm{O}}_{2}↑+{\mathrm{H}}_{2}\mathrm{O}} $ , $ {\rm \mathrm{B}} $ 错误; $ {t}_{1}\mathrm{s} $ 后,外电路中电流方向发生改变,其原因是 $ {\rm \mathrm{A}\mathrm{l}} $ 在浓硝酸中钝化,形成的氧化膜阻止了 $ {\rm \mathrm{A}\mathrm{l}} $ 的进一步反应, $ {\rm \mathrm{C}} $ 正确; $ {t}_{1}\mathrm{s} $ 后, $ {\rm \mathrm{C}\mathrm{u}} $ 为负极,电子从铜片流出经过外电路流向铝片, $ {\rm \mathrm{D}} $ 错误。
9.回答下列问题:
(1) 化学反应中伴随着能量变化,符合如图能量变化的化学反应是 (填序号)。
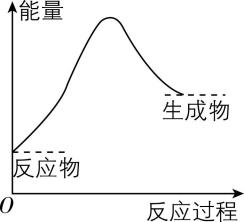
A. 碳酸钙分解
B. 硝酸铵溶于水
C. 氧化铁与 $ {\rm \mathrm{A}\mathrm{l}} $ 高温反应
(2) 在一定温度和压强下,肼 $ {\rm ({\mathrm{N}}_{2}{\mathrm{H}}_{4})} $ 和 $ {\rm {\mathrm{O}}_{2}} $ 发生如下反应: $ {\rm {\mathrm{N}}_{2}{\mathrm{H}}_{4}(\mathrm{g})+{\mathrm{O}}_{2}(\mathrm{g})⇌{\mathrm{N}}_{2}(\mathrm{g})+2{\mathrm{H}}_{2}\mathrm{O}(\mathrm{g})} $ 。已知:肼分子中氮元素为 $ -2 $ 价;断开 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{N}}_{2}{\mathrm{H}}_{4}} $ 和 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{O}}_{2}} $ 中的化学键需分别吸收 $ {\rm 1718\mathrm{k}\mathrm{J}} $ 和 $ {\rm 500\mathrm{k}\mathrm{J}} $ 热量,形成 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{N}}_{2}} $ 和 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{H}}_{2}\mathrm{O}} $ 中的化学键需分别放出 $ {\rm 942\mathrm{k}\mathrm{J}} $ 和 $ {\rm 926\mathrm{k}\mathrm{J}} $ 热量。该反应属于 反应(填“放热”或“吸热”), $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{N}}_{2}{\mathrm{H}}_{4}(\mathrm{g})} $ 和 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{O}}_{2}(\mathrm{g})} $ 的总能量 (填“ $ > $ ”“ $ = $ ”或“ $ < $ ”) $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{N}}_{2}(\mathrm{g})} $ 和 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{H}}_{2}\mathrm{O}(\mathrm{g})} $ 的总能量。
(3) 肼 $ {\rm ({\mathrm{N}}_{2}{\mathrm{H}}_{4})} $ 还是一种良好的火箭推进剂,与助燃剂液态 $ {\rm {\mathrm{N}}_{2}{\mathrm{O}}_{4}} $ 发生反应,放出大量热且对环境无污染,写出该反应的化学方程式: 。
答案:(1) A
(2) 放热; $ > $
(3) $ {\rm 2{\mathrm{N}}_{2}{\mathrm{H}}_{4}+{\mathrm{N}}_{2}{\mathrm{O}}_{4}\xlongequal{点燃}3{\mathrm{N}}_{2}+4{\mathrm{H}}_{2}\mathrm{O}} $
解析:(1) 碳酸钙分解属于吸热反应, $ {\rm \mathrm{A}} $ 符合题意;硝酸铵溶于水属于物理变化,不是化学反应, $ {\rm \mathrm{B}} $ 不符合题意;氧化铁与 $ {\rm \mathrm{A}\mathrm{l}} $ 发生铝热反应,属于放热反应, $ {\rm \mathrm{C}} $ 不符合题意。
(2) 断开 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{N}}_{2}{\mathrm{H}}_{4}} $ 和 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{O}}_{2}} $ 中化学键吸收的热量为 $ {\rm 1718\mathrm{k}\mathrm{J}+500\mathrm{k}\mathrm{J}=2218\mathrm{k}\mathrm{J}} $ ,形成 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{N}}_{2}} $ 和 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{H}}_{2}\mathrm{O}} $ 中化学键放出的热量为 $ {\rm 942\mathrm{k}\mathrm{J}+2×926\mathrm{k}\mathrm{J}=2794\mathrm{k}\mathrm{J} > 2218\mathrm{k}\mathrm{J}} $ ,该反应属于放热反应,即 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{N}}_{2}{\mathrm{H}}_{4}(\mathrm{g})} $ 和 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{O}}_{2}(\mathrm{g})} $ 的总能量 $ {\rm > 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{N}}_{2}(\mathrm{g})} $ 和 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{H}}_{2}\mathrm{O}(\mathrm{g})} $ 的总能量。
(3) $ {\rm {\mathrm{N}}_{2}{\mathrm{H}}_{4}} $ 与助燃剂液态 $ {\rm {\mathrm{N}}_{2}{\mathrm{O}}_{4}} $ 发生反应,放出大量热且对环境无污染,说明产物是氮气和水,该反应的化学方程式为 $ {\rm 2{\mathrm{N}}_{2}{\mathrm{H}}_{4}+{\mathrm{N}}_{2}{\mathrm{O}}_{4}\xlongequal{点燃}3{\mathrm{N}}_{2}+4{\mathrm{H}}_{2}\mathrm{O}} $ 。


















