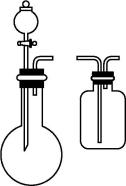
1.活字印刷术极大地促进了世界文化的交流,推动了人类文明的进步。下列“活字”字坯的主要成分为硅酸盐的是( )
|
|
|
|
选项 | 气体 | 试剂 |
A | $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ | 饱和 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $ 溶液 $ + $ 浓硫酸 |
B | $ {\rm {\mathrm{C}\mathrm{l}}_{2}} $ | $ {\rm {\mathrm{M}\mathrm{n}\mathrm{O}}_{2}+} $ 浓盐酸 |
C | $ {\rm {\mathrm{N}\mathrm{H}}_{3}} $ | 固体 $ {\rm {\mathrm{N}\mathrm{H}}_{4}\mathrm{C}\mathrm{l}+} $ 熟石灰 |
D | $ {\rm {\mathrm{C}\mathrm{O}}_{2}} $ | 石灰石 $ + $ 稀盐酸 |
C
饱和 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $ 溶液和浓硫酸反应可以制 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ ,使用固液不加热制气装置, $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 密度比空气大,用向上排空气法收集, $ {\rm \mathrm{A}} $ 不符合题意; $ {\rm {\mathrm{M}\mathrm{n}\mathrm{O}}_{2}} $ 和浓盐酸加热反应可以制 $ {\rm {\mathrm{C}\mathrm{l}}_{2}} $ ,使用固液加热制气装置, $ {\rm {\mathrm{C}\mathrm{l}}_{2}} $ 密度比空气大,用向上排空气法收集, $ {\rm \mathrm{B}} $ 不符合题意;固体 $ {\rm {\mathrm{N}\mathrm{H}}_{4}\mathrm{C}\mathrm{l}} $ 与熟石灰加热可以制 $ {\rm {\mathrm{N}\mathrm{H}}_{3}} $ ,需要使用固固加热制气装置,图中装置不合理, $ {\rm \mathrm{C}} $ 符合题意;石灰石(主要成分为 $ {\rm {\mathrm{C}\mathrm{a}\mathrm{C}\mathrm{O}}_{3}} $ )和稀盐酸反应可以制 $ {\rm {\mathrm{C}\mathrm{O}}_{2}} $ ,使用固液不加热制气装置, $ {\rm {\mathrm{C}\mathrm{O}}_{2}} $ 密度比空气大,用向上排空气法收集, $ {\rm \mathrm{D}} $ 不符合题意。
4.下列实验产生的废液中,可能大量存在的粒子组是( )
选项 | 实验 | 粒子组 |
A | 稀硝酸与铜片制 $ {\rm \mathrm{N}\mathrm{O}} $ | $ {\rm {\mathrm{H}}^{+}} $ 、 $ {\rm {\mathrm{C}\mathrm{u}}^{2+}} $ 、 $ {\rm {\mathrm{N}\mathrm{O}}_{3}^{-}} $ 、 $ {\rm \mathrm{N}\mathrm{O}} $ |
B | $ 70\% $ 硫酸与 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $ 制 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ | $ {\rm {\mathrm{H}}^{+}} $ 、 $ {\rm {\mathrm{N}\mathrm{a}}^{+}} $ 、 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ 、 $ {\rm {\mathrm{H}\mathrm{S}\mathrm{O}}_{3}^{-}} $ |
C | 浓盐酸与 $ {\rm {\mathrm{K}\mathrm{M}\mathrm{n}\mathrm{O}}_{4}} $ 制 $ {\rm {\mathrm{C}\mathrm{l}}_{2}} $ | $ {\rm {\mathrm{H}}^{+}} $ 、 $ {\rm {\mathrm{K}}^{+}} $ 、 $ {\rm {\mathrm{M}\mathrm{n}}^{2+}} $ 、 $ {\rm {\mathrm{C}\mathrm{l}}^{-}} $ |
D | 双氧水与 $ {\rm {\mathrm{F}\mathrm{e}\mathrm{C}\mathrm{l}}_{3}} $ 溶液制 $ {\rm {\mathrm{O}}_{2}} $ | $ {\rm {\mathrm{H}}^{+}} $ 、 $ {\rm {\mathrm{F}\mathrm{e}}^{2+}} $ 、 $ {\rm {\mathrm{C}\mathrm{l}}^{-}} $ 、 $ {\rm {\mathrm{H}}_{2}{\mathrm{O}}_{2}} $ |
C
$ {\rm \mathrm{N}\mathrm{O}} $ 难溶于水,在水溶液体系中不能大量存在, $ {\rm \mathrm{A}} $ 错误; $ {\rm {\mathrm{H}}^{+}} $ 与 $ {\rm {\mathrm{H}\mathrm{S}\mathrm{O}}_{3}^{-}} $ 会发生反应: $ {\rm {\mathrm{H}}^{+}+{\mathrm{H}\mathrm{S}\mathrm{O}}_{3}^{-}\xlongequal{}{\mathrm{S}\mathrm{O}}_{2}↑+{\mathrm{H}}_{2}\mathrm{O}} $ ,无法大量共存, $ {\rm \mathrm{B}} $ 错误;反应后废液中不存在 $ {\rm {\mathrm{M}\mathrm{n}\mathrm{O}}_{4}^{-}} $ 时,生成的 $ {\rm {\mathrm{M}\mathrm{n}\mathrm{C}\mathrm{l}}_{2}} $ 、 $ {\rm \mathrm{K}\mathrm{C}\mathrm{l}} $ 和剩余的 $ {\rm \mathrm{H}\mathrm{C}\mathrm{l}} $ 能共存,故废液中可能大量存在 $ {\rm {\mathrm{H}}^{+}} $ 、 $ {\rm {\mathrm{K}}^{+}} $ 、 $ {\rm {\mathrm{M}\mathrm{n}}^{2+}} $ 、 $ {\rm {\mathrm{C}\mathrm{l}}^{-}} $ , $ {\rm \mathrm{C}} $ 正确; $ {\rm {\mathrm{F}\mathrm{e}}^{2+}} $ 与 $ {\rm {\mathrm{H}}_{2}{\mathrm{O}}_{2}} $ 在酸性条件下会发生氧化还原反应: $ {\rm 2{\mathrm{F}\mathrm{e}}^{2+}+{\mathrm{H}}_{2}{\mathrm{O}}_{2}+2{\mathrm{H}}^{+}\xlongequal{}2{\mathrm{F}\mathrm{e}}^{3+}+2{\mathrm{H}}_{2}\mathrm{O}} $ ,无法大量共存, $ {\rm \mathrm{D}} $ 错误。
5.如图所示的物质转化关系中,固体A与固体B研细后混合,常温下搅拌产生气体C和固体D,温度迅速下降。气体C能使湿润的红色石蕊试纸变蓝。 $ {\rm \mathrm{G}} $ 是一种强酸。 $ {\rm \mathrm{H}} $ 是白色固体,常用作钡餐。下列叙述错误的是( )
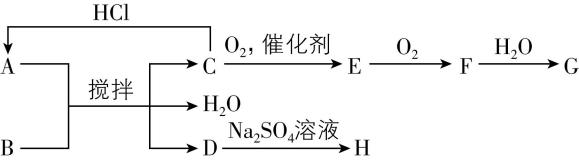
A. 在C的水溶液中加入少量固体A,溶液 $ {\rm \mathrm{p}\mathrm{H}} $ 升高
B. D为可溶于水的有毒物质
C. $ {\rm \mathrm{F}} $ 溶于雨水可形成酸雨
D. 常温下可用铁制容器来盛装 $ {\rm \mathrm{G}} $ 的浓溶液
A
【图解】
由题目信息“气体C能使湿润的红色石蕊试纸变蓝”,可推出气体C为 $ {\rm {\mathrm{N}\mathrm{H}}_{3}} $ ,结合转化关系可知, $ {\rm \mathrm{E}} $ 为 $ {\rm \mathrm{N}\mathrm{O}} $ , $ {\rm \mathrm{F}} $ 为 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ , $ {\rm \mathrm{G}} $ 为 $ {\rm {\mathrm{H}\mathrm{N}\mathrm{O}}_{3}} $ ,符合题目信息“ $ {\rm \mathrm{G}} $ 是一种强酸”。C和 $ {\rm \mathrm{H}\mathrm{C}\mathrm{l}} $ 反应生成 $ {\rm \mathrm{A}({\mathrm{N}\mathrm{H}}_{4}\mathrm{C}\mathrm{l})} $ ,同时 $ {\rm \mathrm{H}} $ 常用作钡餐,推出 $ {\rm \mathrm{H}} $ 为 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{S}\mathrm{O}}_{4} ,A} $ 和B反应得到D,则D为 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{l}}_{2}} $ ,再由题目信息固体A和固体B研细混合,常温下搅拌反应时温度迅速下降,知 $ {\rm \mathrm{A}({\mathrm{N}\mathrm{H}}_{4}\mathrm{C}\mathrm{l})} $ 和B反应吸热,确定B为 $ {\rm \mathrm{B}\mathrm{a}(\mathrm{O}\mathrm{H})_{2}\cdot 8{\mathrm{H}}_{2}\mathrm{O}} $ 。
$ {\rm {\mathrm{N}\mathrm{H}}_{4}\mathrm{C}\mathrm{l}} $ 水溶液显酸性,在氨水(碱性)中加入 $ {\rm {\mathrm{N}\mathrm{H}}_{4}\mathrm{C}\mathrm{l}} $ 固体会使溶液 $ {\rm \mathrm{p}\mathrm{H}} $ 降低, $ {\rm \mathrm{A}} $ 错误; $ {\rm {\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{l}}_{2}(\mathrm{D})} $ 可溶于水,属于重金属盐,有毒, $ {\rm \mathrm{B}} $ 正确; $ {\rm {\mathrm{N}\mathrm{O}}_{2}(\mathrm{F})} $ 溶于水会形成硝酸型酸雨, $ {\rm \mathrm{C}} $ 正确;常温下, $ {\rm \mathrm{F}\mathrm{e}} $ 遇浓硝酸会钝化,故可用铁制容器盛装浓硝酸, $ {\rm \mathrm{D}} $ 正确。
6.按如图组装装置并进行实验:将铜丝插入溶液中,当 $ \mathrm{c} $ 中红色褪去时,将铜丝拔离液面。下列叙述错误的是( )
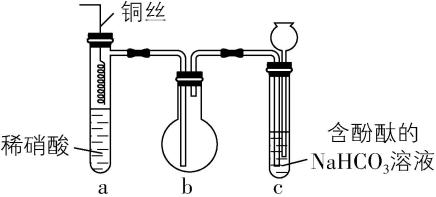
A. $ \mathrm{a} $ 中有化合反应发生,并有颜色变化
B. $ \mathrm{b} $ 中气体变红棕色时,所含氮氧化物至少有两种
C. $ \mathrm{c} $ 中溶液红色刚好褪去时, $ {\rm {\mathrm{H}\mathrm{C}\mathrm{O}}_{3}^{-}} $ 恰好完全反应
D. 若将 $ \mathrm{a} $ 中稀硝酸换为浓硫酸并加热,则 $ \mathrm{c} $ 中溶液颜色会褪去
$ \mathrm{a} $ 中铜与稀硝酸发生反应: $ {\rm 3\mathrm{C}\mathrm{u}+8{\mathrm{H}}^{+}+2{\mathrm{N}\mathrm{O}}_{3}^{-}\xlongequal{}3{\mathrm{C}\mathrm{u}}^{2+}+2\mathrm{N}\mathrm{O}↑+4{\mathrm{H}}_{2}\mathrm{O}} $ ,反应生成的 $ {\rm \mathrm{N}\mathrm{O}} $ 极易与空气中的 $ {\rm {\mathrm{O}}_{2}} $ 发生反应: $ {\rm 2\mathrm{N}\mathrm{O}+{\mathrm{O}}_{2}\xlongequal{}2{\mathrm{N}\mathrm{O}}_{2}} $ ,因此 $ \mathrm{a} $ 中有化合反应发生,且溶液由无色变为蓝色、气体由无色变为红棕色, $ {\rm \mathrm{A}} $ 正确; $ \mathrm{b} $ 中气体变为红棕色时, $ \mathrm{b} $ 中一定存在 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ ,且存在平衡: $ {\rm 2{\mathrm{N}\mathrm{O}}_{2}⇌{\mathrm{N}}_{2}{\mathrm{O}}_{4}} $ ,则 $ \mathrm{b} $ 中也一定存在 $ {\rm {\mathrm{N}}_{2}{\mathrm{O}}_{4}} $ ,所以 $ \mathrm{b} $ 中所含氮氧化物至少有两种, $ {\rm \mathrm{B}} $ 正确; $ \mathrm{b} $ 中的 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 进入 $ \mathrm{c} $ 中,与水发生反应: $ {\rm 3{\mathrm{N}\mathrm{O}}_{2}+{\mathrm{H}}_{2}\mathrm{O}\xlongequal{}2{\mathrm{H}\mathrm{N}\mathrm{O}}_{3}+\mathrm{N}\mathrm{O}} $ ,反应生成的 $ {\rm {\mathrm{H}\mathrm{N}\mathrm{O}}_{3}} $ 与 $ {\rm {\mathrm{N}\mathrm{a}\mathrm{H}\mathrm{C}\mathrm{O}}_{3}} $ 溶液发生反应: $ {\rm {\mathrm{H}}^{+}+{\mathrm{H}\mathrm{C}\mathrm{O}}_{3}^{-}\xlongequal{}{\mathrm{H}}_{2}\mathrm{O}+{\mathrm{C}\mathrm{O}}_{2}↑} $ ,因为酚酞呈粉红色的 $ {\rm \mathrm{p}\mathrm{H}} $ 范围为 $ 8.2\sim 10.0 $ ,所以当溶液红色刚好褪去时,溶液 $ {\rm \mathrm{p}\mathrm{H}} $ 约为 $ 8.2 $ ,呈弱碱性, $ {\rm {\mathrm{N}\mathrm{a}\mathrm{N}\mathrm{O}}_{3}} $ 溶液呈中性,则此时溶液中还有剩余的 $ {\rm {\mathrm{H}\mathrm{C}\mathrm{O}}_{3}^{-}} $ 未反应, $ {\rm \mathrm{C}} $ 错误;若将 $ \mathrm{a} $ 中的稀硝酸换成浓硫酸并加热,则 $ \mathrm{a} $ 中发生反应: $ {\rm \mathrm{C}\mathrm{u}+2{\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}(浓)\xlongequal{△}{\mathrm{C}\mathrm{u}\mathrm{S}\mathrm{O}}_{4}+{\mathrm{S}\mathrm{O}}_{2}↑+2{\mathrm{H}}_{2}\mathrm{O}} $ ,反应生成的 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 进入 $ \mathrm{c} $ 中遇水生成 $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $ ,酸性: $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{3} > {\mathrm{H}}_{2}{\mathrm{C}\mathrm{O}}_{3}} $ ,则 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 足量时,发生反应: $ {\rm {\mathrm{S}\mathrm{O}}_{2}+{\mathrm{H}\mathrm{C}\mathrm{O}}_{3}^{-}\xlongequal{}{\mathrm{H}\mathrm{S}\mathrm{O}}_{3}^{-}+{\mathrm{C}\mathrm{O}}_{2}} $ ,即溶液中溶质为 $ {\rm {\mathrm{N}\mathrm{a}\mathrm{H}\mathrm{S}\mathrm{O}}_{3}} $ , $ {\rm {\mathrm{H}\mathrm{S}\mathrm{O}}_{3}^{-}} $ 电离程度大于水解程度, $ {\rm {\mathrm{N}\mathrm{a}\mathrm{H}\mathrm{S}\mathrm{O}}_{3}} $ 溶液呈酸性,故 $ \mathrm{c} $ 中溶液颜色会褪去, $ {\rm \mathrm{D}} $ 正确。
7.化学小组实验探究 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 与 $ {\rm {\mathrm{A}\mathrm{g}\mathrm{N}\mathrm{O}}_{3}} $ 溶液的反应。
(1) 实验一:用如下装置(夹持、加热仪器略)制备 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ ,将足量 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 通入 $ {\rm {\mathrm{A}\mathrm{g}\mathrm{N}\mathrm{O}}_{3}} $ 溶液中,迅速反应,得到无色溶液A和白色沉淀B。
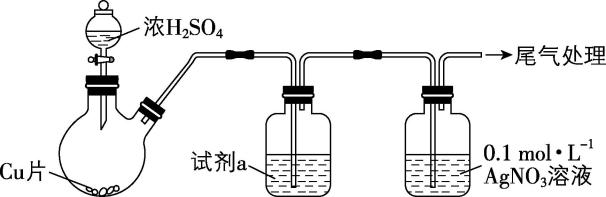
① 浓 $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ 与 $ {\rm \mathrm{C}\mathrm{u}} $ 反应的化学方程式是 。
② 试剂 $ \mathrm{a} $ 是 。
(2) 对体系中有关物质性质分析得出:沉淀B可能为 $ {\rm {\mathrm{A}\mathrm{g}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $ 、 $ {\rm {\mathrm{A}\mathrm{g}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ 或二者混合物。
(资料: $ {\rm {\mathrm{A}\mathrm{g}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ 微溶于水; $ {\rm {\mathrm{A}\mathrm{g}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $ 难溶于水)
实验二:验证B的成分
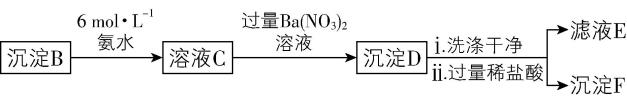
① 写出 $ {\rm {\mathrm{A}\mathrm{g}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $ 溶于氨水生成 $ {\rm \mathrm{A}\mathrm{g}({\mathrm{N}\mathrm{H}}_{3})_{2}^{+}} $ 的离子方程式: 。
② 加入盐酸后沉淀D大部分溶解,剩余少量沉淀 $ {\rm \mathrm{F}} $ 。推断D中主要是 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{S}\mathrm{O}}_{3}} $ ,进而推断B中含有 $ {\rm {\mathrm{A}\mathrm{g}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $ 。向滤液 $ {\rm \mathrm{E}} $ 中加入一种试剂,可进一步证实B中含有 $ {\rm {\mathrm{A}\mathrm{g}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $ 。所用试剂及现象是 。
(3) 根据沉淀 $ {\rm \mathrm{F}} $ 的存在,推测 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ 的产生有两个途径:
途径1:实验一中, $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 在 $ {\rm {\mathrm{A}\mathrm{g}\mathrm{N}\mathrm{O}}_{3}} $ 溶液中被氧化生成 $ {\rm {\mathrm{A}\mathrm{g}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ ,随沉淀B进入D。
途径2:实验二中, $ {\rm {\mathrm{S}\mathrm{O}}_{3}^{2-}} $ 被氧化为 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ 进入D。
实验三:探究 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ 的产生途径
① 向溶液A中滴入过量盐酸,产生白色沉淀,证明溶液中含有 ;取上层清液继续滴加 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{l}}_{2}} $ 溶液,未出现白色沉淀,可判断B中不含 $ {\rm {\mathrm{A}\mathrm{g}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ 。做出判断的理由: 。
② 实验三的结论: 。
(4) 实验一中 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 与 $ {\rm {\mathrm{A}\mathrm{g}\mathrm{N}\mathrm{O}}_{3}} $ 溶液反应的离子方程式是 。
(5)根据物质性质分析, $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 与 $ {\rm {\mathrm{A}\mathrm{g}\mathrm{N}\mathrm{O}}_{3}} $ 溶液应该可以发生氧化还原反应。将实验一所得混合物放置一段时间,有 $ {\rm \mathrm{A}\mathrm{g}} $ 和 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ 生成。
(6) 根据上述实验所得结论: 。
① $ {\rm \mathrm{C}\mathrm{u}+2{\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}(浓)\xlongequal{△}{\mathrm{C}\mathrm{u}\mathrm{S}\mathrm{O}}_{4}+{\mathrm{S}\mathrm{O}}_{2}↑+2{\mathrm{H}}_{2}\mathrm{O}} $
② 饱和 $ {\rm {\mathrm{N}\mathrm{a}\mathrm{H}\mathrm{S}\mathrm{O}}_{3}} $ 溶液
(2) ① $ {\rm {\mathrm{A}\mathrm{g}}_{2}{\mathrm{S}\mathrm{O}}_{3}+4{\mathrm{N}\mathrm{H}}_{3}\cdot {\mathrm{H}}_{2}\mathrm{O}\xlongequal{}2\mathrm{A}\mathrm{g}({\mathrm{N}\mathrm{H}}_{3})_{2}^{+}+{\mathrm{S}\mathrm{O}}_{3}^{2-}+4{\mathrm{H}}_{2}\mathrm{O}} $
② $ {\rm {\mathrm{H}}_{2}{\mathrm{O}}_{2}} $ 溶液,产生白色沉淀
(3) ① $ {\rm {\mathrm{A}\mathrm{g}}^{+}} $ ; $ {\rm {\mathrm{A}\mathrm{g}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ 溶解度大于 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{S}\mathrm{O}}_{4}} $ ,没有 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{S}\mathrm{O}}_{4}} $ 沉淀时,必定没有 $ {\rm {\mathrm{A}\mathrm{g}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $
② 途径1不产生 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ ,途径2产生 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $
(4) $ {\rm 2{\mathrm{A}\mathrm{g}}^{+}+{\mathrm{S}\mathrm{O}}_{2}+{\mathrm{H}}_{2}\mathrm{O}\xlongequal{}{\mathrm{A}\mathrm{g}}_{2}{\mathrm{S}\mathrm{O}}_{3}↓+2{\mathrm{H}}^{+}} $
(6) 实验条件下: $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 与 $ {\rm {\mathrm{A}\mathrm{g}\mathrm{N}\mathrm{O}}_{3}} $ 溶液生成 $ {\rm {\mathrm{A}\mathrm{g}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $ 的速率大于生成 $ {\rm \mathrm{A}\mathrm{g}} $ 和 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ 的速率;碱性溶液中 $ {\rm {\mathrm{S}\mathrm{O}}_{3}^{2-}} $ 更易被氧化为 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $
① 实验室利用浓 $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ 与 $ {\rm \mathrm{C}\mathrm{u}} $ 片在加热条件下反应制取 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ ,化学方程式为 $ {\rm \mathrm{C}\mathrm{u}+2{\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}(浓)\xlongequal{△}{\mathrm{C}\mathrm{u}\mathrm{S}\mathrm{O}}_{4}+{\mathrm{S}\mathrm{O}}_{2}↑+2{\mathrm{H}}_{2}\mathrm{O}} $ 。
② 试剂 $ \mathrm{a} $ 是饱和 $ {\rm {\mathrm{N}\mathrm{a}\mathrm{H}\mathrm{S}\mathrm{O}}_{3}} $ 溶液,用于观察气体流速,且 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 在饱和 $ {\rm {\mathrm{N}\mathrm{a}\mathrm{H}\mathrm{S}\mathrm{O}}_{3}} $ 溶液中溶解度很小,可防止发生倒吸。
(2) ① $ {\rm {\mathrm{A}\mathrm{g}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $ 溶于氨水生成 $ {\rm \mathrm{A}\mathrm{g}({\mathrm{N}\mathrm{H}}_{3})_{2}^{+}} $ ,离子方程式为 $ {\rm {\mathrm{A}\mathrm{g}}_{2}{\mathrm{S}\mathrm{O}}_{3}+4{\mathrm{N}\mathrm{H}}_{3}\cdot {\mathrm{H}}_{2}\mathrm{O}\xlongequal{}2\mathrm{A}\mathrm{g}({\mathrm{N}\mathrm{H}}_{3})_{2}^{+}+{\mathrm{S}\mathrm{O}}_{3}^{2-}+4{\mathrm{H}}_{2}\mathrm{O}} $ 。
② 沉淀 $ {\rm \mathrm{D}} $ 洗涤干净后,加入过量稀盐酸, $ {\rm {\mathrm{B}\mathrm{a}\mathrm{S}\mathrm{O}}_{3}} $ 与稀盐酸反应生成 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{l}}_{2}} $ 、 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 和 $ {\rm {\mathrm{H}}_{2}\mathrm{O}} $ ,则滤液 $ {\rm \mathrm{E}} $ 中含有 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{l}}_{2}} $ 和溶解在水中的 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 形成的 $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $ ,可向 $ {\rm \mathrm{E}} $ 中加入 $ {\rm {\mathrm{H}}_{2}{\mathrm{O}}_{2}} $ 溶液, $ {\rm {\mathrm{H}}_{2}{\mathrm{O}}_{2}} $ 将 $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $ 氧化生成 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ , $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ 和 $ {\rm {\mathrm{B}\mathrm{a}}^{2+}} $ 反应产生 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{S}\mathrm{O}}_{4}} $ 白色沉淀,进一步证实 $ {\rm \mathrm{B}} $ 中含有 $ {\rm {\mathrm{A}\mathrm{g}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $ 。
(3) 向溶液 $ {\rm \mathrm{A}} $ 中滴入过量盐酸,产生白色沉淀,该沉淀为 $ {\rm \mathrm{A}\mathrm{g}\mathrm{C}\mathrm{l}} $ ,证明溶液 $ {\rm \mathrm{A}} $ 中含有 $ {\rm {\mathrm{A}\mathrm{g}}^{+}} $ ;取上层清液继续滴加 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{l}}_{2}} $ 溶液,未出现白色沉淀,证明溶液 $ {\rm \mathrm{A}} $ 中不含 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ ,由于 $ {\rm {\mathrm{A}\mathrm{g}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ 微溶于水,则 $ {\rm \mathrm{B}} $ 中不含 $ {\rm {\mathrm{A}\mathrm{g}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ ,从而确定途径1不产生 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ ,途径2产生 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ 。
(4) 由(3)推知,实验一中 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 与 $ {\rm {\mathrm{A}\mathrm{g}\mathrm{N}\mathrm{O}}_{3}} $ 溶液反应生成 $ {\rm {\mathrm{A}\mathrm{g}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $ ,离子方程式为 $ {\rm 2{\mathrm{A}\mathrm{g}}^{+}+{\mathrm{S}\mathrm{O}}_{2}+{\mathrm{H}}_{2}\mathrm{O}\xlongequal{}{\mathrm{A}\mathrm{g}}_{2}{\mathrm{S}\mathrm{O}}_{3}↓+2{\mathrm{H}}^{+}} $ 。
(6) 对比分析 $ (4)(5) $ 可知, $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 与 $ {\rm {\mathrm{A}\mathrm{g}\mathrm{N}\mathrm{O}}_{3}} $ 溶液反应生成 $ {\rm {\mathrm{A}\mathrm{g}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $ 的速率大于生成 $ {\rm \mathrm{A}\mathrm{g}} $ 和 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ 的速率,再结合实验二可知,碱性溶液中 $ {\rm {\mathrm{S}\mathrm{O}}_{3}^{2-}} $ 更易被氧化为 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ 。